Apr. 01, 2025
木塚 康彦
氏名:木塚 康彦
岐阜大学 糖鎖生命コア研究所(iGCORE)教授
2004年 京都大学薬学部卒、2009年 同博士課程修了、博士(薬学)。2009年より8年半、理化学研究所 谷口直之先生のグループで研究員として勤務、2017年10月より岐阜大学 生命の鎖統合研究センター准教授。2022年より現職。2017年 日本生化学会奨励賞。糖転移酵素の発現、活性調節を生化学的アプローチで研究している。
序文
本稿では、糖鎖とアルツハイマー病の関係について紹介する。認知症の大部分を占めるアルツハイマー病の病態解明や早期診断法の開発は、言うまでもなく、現代社会において急務の課題である。ここでは、糖鎖とアルツハイマー病の関連について、近年の網羅的な糖鎖解析からわかってきたこと、また個別の糖鎖に焦点を当てた研究例について紹介する。これらの研究を通じて、糖鎖を標的としたアルツハイマー病の診断、治療の開発の可能性などについて考えたい。
1. はじめに
日本は超高齢社会を迎えている。現在、65歳以上が人口に占める割合は約29%であり、2070年には40%近くに達すると見込まれている(内閣府、令和6年版高齢社会白書 https://www8.cao.go.jp/kourei/whitepaper/w-2024/html/zenbun/index.html)。この高齢社会にあって、国民の健康ひいては日本の医療と経済を脅かす最大の敵の一つが認知症であり、認知症の大部分を占めるアルツハイマー病(Alzheimer’s disease, AD)の克服は、現代医学が解決すべき大きな課題の一つである。
ADは、進行性の神経変性疾患であり、記憶障害、思考力低下などを症状とする1,2。その治療薬としては、進行を遅らせる抗体医薬品などの開発が進んでいるものの、根本的な治療薬はいまだにないのが現状である。この疾患の治療を困難にしている要因の一つは、原因と考えられる脳内変化が、20年という非常に長いスパンで進行することである。臨床症状を呈した段階では、後述の病理変化がすでに進行しているため、いかに症状を呈さない段階で診断できるかが今後の鍵になると考えられる3,4。また、リスクとなる遺伝子型はあるものの、ほとんどが孤発性で様々な因子が複合的に発症に関わることから1,2、病態に至る分子メカニズムはまだ十分に解明されていない。本稿では、糖鎖の視点から、ADの診断、治療の可能性について議論したい。糖鎖の解析については、近年、糖鎖や糖ペプチド糖鎖の網羅的な構造解析法が著しい発展を遂げつつあり、AD患者における糖鎖の変化やその役割についての研究も進展を見せている。以降のセクションでは、まず、糖鎖の網羅的な解析から見えてきた現状を紹介したい。続いて、個別の糖鎖に焦点を当てた研究、具体的には、筆者らも研究しているbisecting GlcNAc、またO-GlcNAc、GM1ガングリオシド、O-GalNAc型糖鎖、について、ADとの関連性について紹介する。
AD患者の脳では、「老人斑」と「神経原線維変化」という2つの主要な病理変化が見られる1,2。老人斑は、アミロイドβ(Aβ)と呼ばれるペプチドが細胞外に凝集したものであり、神経原線維変化は、異常にリン酸化されたタウ(Tau)タンパク質が細胞内に蓄積したものである(図 1)。両者の間の明確な因果関係はまだ明らかになっていないが、Aβの蓄積が先行すること1,2、家族性ADの原因遺伝子は全てAβの産生や蓄積に関わるタンパク質をコードすることから5、Aβの蓄積が上流となってADを引き起こすとする説が広く支持されている6。Aβは、APP (amyloid precursor protein)と呼ばれるタンパク質が、BACE1 (beta-site APP cleaving enzyme-1)とγ-secretaseによって段階的に切断を受けることによって生じる(図 1)7。またAβとタウは存在する細胞内区画が異なり、Aβがエンドソームなどの内腔側で産生されて分泌される一方、タウは基本的にサイトゾルに局在する(最近では分泌されたタウも注目されている)。すなわち、Aβの産生や凝集に関わるタンパク質群は分泌経路内もしくは細胞外に配向しており、タウに関連するタンパク質は細胞質側に配向する。すなわち糖鎖付加の観点では、Aβ関連タンパク質はN型糖鎖やO型糖鎖で修飾され、タウ関連タンパク質(タウ自身を含む)はO-GlcNAc修飾を受ける。本稿では、これら糖タンパク質に付加された糖鎖を中心に紹介し、さらにガングリオシドの一つであるGM1とADの関係性についても述べたい。
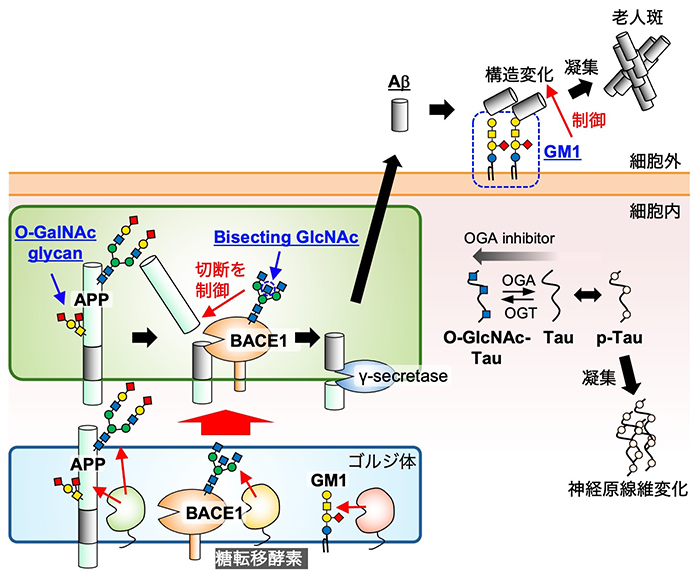 図 1. ADの主要病理変化の原因分子と関連する糖鎖
図 1. ADの主要病理変化の原因分子と関連する糖鎖
ADでは、細胞外にAβが蓄積して老人斑を、細胞内にリン酸化タウが蓄積して神経原線維変化を生じる。Aβは、APPがBACE1、γ-secretaseによって二段階の切断を受けて生じる。APPのO-GalNAc型糖鎖、BACE1のbisecting GlcNAcはAβ産生と関わる。細胞表面の糖脂質の一つGM1はAβと結合し、Aβの凝集過程に関わると考えられる。タウは細胞質でO-GlcNAc化され、O-GlcNAc化を亢進させるとリン酸が抑制されて凝集を抑えられると報告されている。
2. ADにおける網羅的糖鎖解析
近年、質量分析(MS)を用いた網羅的な糖鎖構造解析の手法開発が進んだことで、細胞、組織、タンパク質中の全体的な糖鎖構造情報が得られるようになっており、それをコホートに応用した大規模な研究が可能になってきている。これらの分析手法は、試料中の糖鎖を切り出して糖鎖のみの構造情報を網羅的に得るグライコミクスと、糖鎖が結合したままタンパク質を糖ペプチドに切断して、糖鎖付加部位ごとの糖鎖構造情報を得るグライコプロテオミクスに大別される。後者の方が得られる情報量は多い一方で、現状では多くのケースで解析できる糖鎖がN型糖鎖に限られるという技術的課題も存在する。
ADについても、糖鎖の変動パターン(グライコミクス)と、タンパク質の情報を合わせた糖鎖変動パターン(グライコプロテオミクス)を解析した研究が近年どちらも行われており、糖鎖を標的としたADのバイオマーカー開発への応用が期待される。またサンプルについては、脳脊髄液(cerebrospinal fluid, CSF)を用いた解析が多く、血液、死後脳を用いた解析例もある。CSFを解析したグライコミクスの研究例では、数十例の健常者、軽度認知障害(MCI)、AD患者のCSFを用いた解析が行われている8,9。その結果、健常者と比較して、MCIやADの患者における幾つかの糖鎖変化が見出されており、後述のbisecting GlcNAcを持つ糖鎖の増加や、シアル酸の低下などが共通して観察されている8,9。また、フコシル化糖鎖の増加を報告している例もある10。AD患者の死後脳をLC-MSでグライコミクス解析した研究においても、複数の糖鎖の変動が検出されているものの、特定の共通する糖鎖構造モチーフの変化は抽出されていない11。
グライコプロテオミクス解析では、Chenらが、健常者とAD患者のCSFを用いた解析により3,000近い糖ペプチドの同定を行っており、ADにおける特定の糖タンパク質上のN型糖鎖構造変化を報告している12。また、AD患者の脳サンプルを用いたグライコプロテオミクス解析も行われている。Suttapitugsakulらは、2,000以上の糖ペプチドを同定しており、ADにおける全体的な糖鎖構造パターンの変化、サイトごとの糖鎖構造の変化などを報告している13。さらに2024年の研究では、12,000を超える糖ペプチドがAD患者の脳から同定され、より詳細なサイトごとの糖鎖変化が明らかになってきている14。また、糖鎖構造ではなく、N型糖鎖の付加効率などを分析している例もあり、AD脳サンプルを用いたLC-MS解析により、タンパク質内のN型糖鎖の付加の有無や、同一サイトの糖鎖付加効率に違いがあることもわかってきている15。以上のような網羅的なグライコミクス、グライコプロテオミクス解析では、同定できる情報量が日に日に増してきている。今後は、多くの検体を含むコホートサンプルを用いた大規模解析が行われていくと考えられる。
3. Bisecting GlcNAcとAD
Bisecting GlcNAcは、N型糖鎖中央のβ-Manに結合した GlcNAc残基のことを指し、この構造はGnT-III(MGAT3)と呼ばれる酵素によって作られる16。Bisecting GlcNAcは、N型糖鎖の他の分岐や末端構造の形成を抑制する機能があるほか17,18、がんの悪性化を抑制する働きなども報告されている19。一方、Bisecting GlcNAcを合成するGnT-IIIの発現は脳で強く、特にニューロンでの発現が高い20。ニューロンや脳におけるbisecting GlcNAcの役割については不明であったが、2010年、遠藤らのグループが、AD患者でGnT-IIIのmRNAレベルが増加していることをヒト脳の解析により明らかにした21。これにより、bisecting GlcNAcとADとの関連が示唆されたことから、我々は、GnT-III欠損マウスにおいてAD病態がどのように変化するのかを解析した。
マウスはADを自然発症しないため、ADの研究ではモデルマウスが用いられる22。我々は、AD研究でよく用いられる、家族性ADの変異を持つヒトAPPのトランスジェニックマウス(以下APP-Tg)とGnT-III欠損マウスを交配して解析を行った。その結果、加齢とともに脳内で観察される老人斑の数が、GnT-III欠損APP-Tgでは激減していた23。さらに、Y迷路を用いた認知能力の試験においても、APP-Tgで見られる成績低下が、GnT-III欠損APP-Tgでは野生型に近いレベルまで回復していた。以上から、bisecting GlcNAcの欠損は、脳内Aβ蓄積量の減少とAD病態の改善をもたらすことがわかった。
次の疑問は、bisecting GlcNAcの欠損によりAβ量が減少するメカニズムである。Aβは上述のように、APPが2段階の切断を受けて生じるが(図 1)、このAPPの代謝経路中のタンパク質はほとんどがN型糖鎖修飾を受ける24。これらの糖タンパク質の糖鎖を調べたところ、APPの一段階目の切断を担う酵素BACE1の糖鎖がbisecting GlcNAc構造を多く持つことがわかった。そこでBACE1の機能について解析した結果、BACE1によるAPP切断産物の量が、GnT-III欠損APP-Tgマウスでは有意に減少していた。このことから、bisecting GlcNAcの欠損はBACE1の機能低下を引き起こすことが明らかになった。さらにBACE1の性質を詳細に調べたところ、bisecting GlcNAcを欠損してもBACE1の切断活性自体はほとんど変化しなかった一方で、BACE1の細胞内局在は、GnT-IIIの欠損により初期エンドソームから後期エンドソームとリソソームへ移行していることがわかった。BACE1によるAPPの切断には、初期エンドソームへの局在が重要との報告がなされていることから25,26、このBACE1の局在変化がAβ産生低下の原因であると考えられた。以上のことから、bisecting GlcNAcは、BACE1の局在制御を介してAβ産生を正に調節しており、新たなAD治療標的となる可能性が考えられた。しかし、なぜ糖鎖の欠損によってBACE1の局在が変化するのかはまだ明らかになっておらず、今後解決すべき課題である。
Bisecting GlcNAcは、上述のCSFのグライコミクス解析において、MCI患者、AD患者において増加が見られた8,10。さらに、レクチンを用いたELISAの系により、CSF中のbisecting GlcNAcの検出がADの診断や早期の認知能力低下の指標として利用できる可能性も示唆されている27,28。また、血液中のbisecting GlcNAcが、タウのレベルやAPOEの遺伝子型の組み合わせにより、ADの診断に使用できる可能性も示唆されており29、今後のさらなる解析が期待される。
4. O-GlcNAcとAD
O-GlcNAcはSer/ThrにGlcNAc単糖が付加する翻訳後修飾であり、細胞質、核、ミトコンドリアで起こる30。1,000を超えるタンパク質がO-GlcNAc修飾されることが知られており、ADとの関連では、タウのO-GlcNAc修飾がよく研究されている31,32。タウは多くの部位でリン酸化を受けるタンパク質で、異常にリン酸化されたタウの凝集体が神経原線維変化の本体である33。一般に、O-GlcNAc化とリン酸化は共にSer/Thr残基で起こり、しばしば互いに競合することから30,34、タウのリン酸化もO-GlcNAc化によって制御されている可能性が示唆されていた。Yuzwaらは、O-GlcNAc分解酵素の阻害剤を用い、O-GlcNAcレベルの上昇によりタウのリン酸化が減少することを報告している31。さらに、変異タウ(P301L)マウスにおいて、O-GlcNAcレベルの増加がタウのリン酸化と凝集を抑制し、病態が改善することが示されている35,36。これらの知見は、O-GlcNAcレベルの増加がADに対して治療効果をもたらす可能性を示唆している。一方、上述したように、O-GlcNAc修飾は数多くのタンパク質に普遍的に発現しているため、O-GlcNAcレベルの全身的な変化は多くのタンパク質の機能的変化を引き起こす可能性がある。そのため、O-GlcNAcを標的としたAD治療には、その点に留意した研究が必要であると考えられる。
また、サイトゾルに存在するタウはN型糖鎖修飾を通常受けないと考えられるが、AD患者では、タウが異常にN型糖鎖修飾される可能性が報告されている15,37,38。また、経路はまだはっきりしていないが、血中に分泌されたタウの早期診断マーカーとしての有用性も近年検証されている。今後、糖ペプチドの構造解析によって、タウがAD依存的にN型糖鎖付加を受けることが明確になれば、その異常な糖鎖付加は、基礎的な糖鎖付加やタウの分泌経路の仕組みの理解に加え、ADの新たな治療標的開発という観点からも重要な研究対象になる可能性がある。
5. GM1ガングリオシドとAD
GM1はADに関与することが報告されているガングリオシドであり、Aβ 凝集のseedとしてADの病態形成を促す役割が報告されている39,40ほか、その一方でADの神経変性に対して保護的に働くとの報告もある41。柳沢らのグループは、初期のAD患者の脳で、GM1と結合したAβ を見出している42。その後、多くのin vitroおよびin vivoの研究から、GM1と結合したAβが凝集体形成のseedとして機能することが示唆された。例えば、単量体AβがGM1を含む様々なガングリオシドと結合すること43、GM1-Aβの相互作用がGM1の脂質部分の組成やクラスター状態に依存していること44、またNMRにより、Aβ がGM1のクラスターに結合するとコンフォメーションがα-helixからβ-sheetの状態に移行し、Aβの線維化を引き起こすこと45,46、などが示されている。さらに、APP-Tgマウスの脳とヒトのCSFにおいても、GM1と結合したAβが検出されている47,48。また、ADモデルマウスにおいてガングリオシドの分解を薬剤で亢進させると、ガングリオシドに結合したAβ のレベルが低下し、マウスの行動試験の成績も改善した49。これらの知見は、GM1などのガングリオシドがAβと相互作用することで、病態形成に対して促進的に働くことを示している。
一方、GM1関連酵素を標的とした遺伝子改変マウスなどの研究結果は複雑であり、慎重な解釈が必要である。GM2合成酵素(B4GALNT1)を欠損させたB4galnt1 KOマウスでは、GM1が消失してGM3が蓄積するが、Aβの蓄積量は増加していた50。一方、培養細胞を用いた研究では、B4GALNT1の過剰発現によってGM1を増加させると、BACE1のタンパク質量が増加することが示されている51。このことは、GM1がAβの凝集だけでなく産生のプロセスにも影響していることを示唆している。また、GM1やGM3を含む多くのガングリオシドの合成に必要なST3GAL5を欠損させたマウスでは、Aβ の蓄積量が有意に少なくなり、認知試験の成績も向上した52。このような複雑な結果が見られる理由はまだ不明であるが、多くのガングリオシドが異なる親和性でAβに結合することや、一つの生合成酵素の過剰発現や欠失が複数の糖脂質のレベルに影響を及ぼすことと関係しているのかもしれない。
6. O-GalNAc型糖鎖とAD
O-GalNAc型糖鎖は主要なO型糖鎖であり、複数のAD関連分子に付加している。特に、APPのO-GalNAc型糖鎖修飾についてはよく研究されており、例えばヒトCSF中のAPPにおいて多くのO-GalNAc型糖鎖修飾部位が同定されている53,54。ヒトのAPPは、BACE1による切断部位近傍で特にO-GalNAc型糖鎖修飾を受けていることから、APP上のO-GalNAc型糖鎖は、その構造によりAβの生成に影響を与えうると考えられる。
O-GalNAc型糖鎖の生合成は、Ser/Thr残基へのGalNAcの転移により開始され、この過程はGALNTと呼ばれる酵素群により触媒される55。萬谷らのグループは、20のGALNTのうち、いくつかの酵素のmRNAレベルがAD患者脳において上昇していることを報告している56。これらの発現上昇した酵素の一つであるGALNT6を培養細胞で過剰発現させると、培養上清中に分泌されるAβ量が減少していた。この分子機構はまだ不明な点が多いが、少なくともin vitroのアッセイにおいて、GALNT6はBACE1による切断部位に近いAPPのペプチドにGalNAcを転移する活性が示されている56。
興味深いことに、APPはニューロン型(695)と血管内皮細胞型(770)の異なるアイソフォームとして発現しており、これらのアイソフォームはO-GalNAc型糖鎖による修飾過程が異なることがわかってきた。北爪らは、血管内皮細胞に発現するAPP770では、O-GalNAc型糖鎖が付加したものと付加していないグライコフォームのうち、付加したものから選択的にAβが産生されること57、さらにAPP770では、いったん細胞表面に輸送されたAPPがエンドサイトーシスされる過程でO-GalNAc型糖鎖修飾を受けること58、を報告している。AD患者では、高頻度に血管にもAβが沈着し、脳アミロイドアンギオパチーと呼ばれる病態を呈することから59、血管内皮細胞のAPPの特徴的な糖鎖付加過程は、ADの病態形成に関わる可能性がある。また興味深いことに、AβのTyr残基上のO-GalNAc型糖鎖がCSFで発見されている54。このようなAPPのユニークな糖鎖修飾について、その仕組みとADにおける役割の全容解明が今後期待される。
7. その他の糖タンパク質の糖鎖とADとの関連性
TREM2は、骨髄系の細胞に発現する一回膜貫通型タンパク質であり、ゲノムワイド関連解析(GWAS)においてADと関連することが示されている60。その分子機能としては、APOE、脂質、核酸を含む様々な分子の受容体として働くことが明らかになっている61。また、AD患者およびモデルマウスにおいて、TREM2の発現増加が確認されている62,63。興味深いことに、ADのリスク因子であるTREM2のR47H変異は、TREM2のリガンド結合活性を低下させるだけでなく64、TREM2のN型糖鎖の構造変化を引き起こし、シアリル化やフコシル化のパターンを変化させることが報告されている65。また変異型TREM2では、リソソームにおける分解が亢進していたことから、TREM2上のN型糖鎖がその安定性やリガンド結合性、ひいてはAD病態に関与している可能性も考えられる。
8. おわりに
本稿では、ADの発症や進行に関与する様々な糖鎖の研究について紹介した。これらの知見は、変化した糖鎖やその生合成酵素がADのバイオマーカーとして利用できる可能性や、これらの糖鎖の発現や機能を調節することで治療効果が得られる可能性を示している。最近では、脳のグリコーゲン中にグルコサミンが大量に含まれており、UDP-GlcNAcの供給源となって、これが糖鎖発現や認知機能と関わることが報告されており66、脳の糖鎖発現の様式について新たな側面が見えてきている。今後、AD関連糖鎖を特異的に検出する手法、またそれら糖鎖の生合成や機能を選択的に変化させる薬剤や手法の開発が望まれる。
謝辞
本稿で紹介したGnT-III欠損マウスの研究は、谷口直之先生が主宰されていた理化学研究所疾患糖鎖研究チームで行ったものです。ご指導いただいた谷口先生、北爪しのぶ先生に感謝申し上げます。また本稿の執筆にあたり、名古屋市立大学の斉藤貴志先生にご助言をいただきました。この場を借りて感謝申し上げます。
References
- Scheltens, P., Blennow, K., Breteler, M. M., de Strooper, B., Frisoni, G. B., Salloway, S., and Van der Flier, W. M. (2016) Alzheimer's disease. Lancet 388, 505-517
- Selkoe, D. J. (2011) Resolving controversies on the path to Alzheimer's therapeutics. Nat Med 17, 1060-1065
- Porteri, C., Albanese, E., Scerri, C., Carrillo, M. C., Snyder, H. M., Martensson, B., Baker, M., Giacobini, E., Boccardi, M., Winblad, B., Frisoni, G. B., Hurst, S., and Geneva Task Force for the Roadmap of Alzheimer's, B. (2017) The biomarker-based diagnosis of Alzheimer's disease. 1-ethical and societal issues. Neurobiol Aging 52, 132-140
- Lazarczyk, M. J., Hof, P. R., Bouras, C., and Giannakopoulos, P. (2012) Preclinical Alzheimer disease: identification of cases at risk among cognitively intact older individuals. BMC Med 10, 127
- Rogaev, E. I., Sherrington, R., Rogaeva, E. A., Levesque, G., Ikeda, M., Liang, Y., Chi, H., Lin, C., Holman, K., Tsuda, T., and et al. (1995) Familial Alzheimer's disease in kindreds with missense mutations in a gene on chromosome 1 related to the Alzheimer's disease type 3 gene. Nature 376, 775-778
- Karran, E., Mercken, M., and De Strooper, B. (2011) The amyloid cascade hypothesis for Alzheimer's disease: an appraisal for the development of therapeutics. Nat Rev Drug Discov 10, 698-712
- Haass, C., Kaether, C., Thinakaran, G., and Sisodia, S. (2012) Trafficking and proteolytic processing of APP. Cold Spring Harb Perspect Med 2, a006270
- Palmigiano, A., Barone, R., Sturiale, L., Sanfilippo, C., Bua, R. O., Romeo, D. A., Messina, A., Capuana, M. L., Maci, T., Le Pira, F., Zappia, M., and Garozzo, D. (2016) CSF N-glycoproteomics for early diagnosis in Alzheimer's disease. J Proteomics 131, 29-37
- Schedin-Weiss, S., Gaunitz, S., Sui, P., Chen, Q., Haslam, S. M., Blennow, K., Winblad, B., Dell, A., and Tjernberg, L. O. (2019) Glycan biomarkers for Alzheimer disease correlate with T-tau and P-tau in cerebrospinal fluid in subjective cognitive impairment. FEBS J
- Cho, B. G., Veillon, L., and Mechref, Y. (2019) N-Glycan Profile of Cerebrospinal Fluids from Alzheimer's Disease Patients Using Liquid Chromatography with Mass Spectrometry. J Proteome Res 18, 3770-3779
- Gaunitz, S., Tjernberg, L. O., and Schedin-Weiss, S. (2021) The N-glycan profile in cortex and hippocampus is altered in Alzheimer disease. J Neurochem 159, 292-304
- Chen, Z., Yu, Q., Yu, Q., Johnson, J., Shipman, R., Zhong, X., Huang, J., Asthana, S., Carlsson, C., Okonkwo, O., and Li, L. (2021) In-depth Site-specific Analysis of N-glycoproteome in Human Cerebrospinal Fluid and Glycosylation Landscape Changes in Alzheimer's Disease. Mol Cell Proteomics 20, 100081
- Suttapitugsakul, S., Stavenhagen, K., Donskaya, S., Bennett, D. A., Mealer, R. G., Seyfried, N. T., and Cummings, R. D. (2022) Glycoproteomics Landscape of Asymptomatic and Symptomatic Human Alzheimer's Disease Brain. Mol Cell Proteomics 21, 100433
- Zhang, Q., Ma, C., Chin, L. S., Pan, S., and Li, L. (2024) Human brain glycoform coregulation network and glycan modification alterations in Alzheimer's disease. Sci Adv 10, eadk6911
- Zhang, Q., Ma, C., Chin, L. S., and Li, L. (2020) Integrative glycoproteomics reveals protein N-glycosylation aberrations and glycoproteomic network alterations in Alzheimer's disease. Sci Adv 6
- Nishikawa, A., Ihara, Y., Hatakeyama, M., Kangawa, K., and Taniguchi, N. (1992) Purification, cDNA cloning, and expression of UDP-N-acetylglucosamine: beta-D-mannoside beta-1,4N-acetylglucosaminyltransferase III from rat kidney. J Biol Chem 267, 18199-18204
- Schachter, H. (1986) Biosynthetic controls that determine the branching and microheterogeneity of protein-bound oligosaccharides. Biochem Cell Biol 64, 163-181
- Nakano, M., Mishra, S. K., Tokoro, Y., Sato, K., Nakajima, K., Yamaguchi, Y., Taniguchi, N., and Kizuka, Y. (2019) Bisecting GlcNAc Is a General Suppressor of Terminal Modification of N-glycan. Mol Cell Proteomics 18, 2044-2057
- Taniguchi, N., and Kizuka, Y. (2015) Glycans and cancer: role of N-glycans in cancer biomarker, progression and metastasis, and therapeutics. Adv Cancer Res 126, 11-51
- Kizuka, Y., Nakano, M., Miura, Y., and Taniguchi, N. (2016) Epigenetic regulation of neural N-glycomics. Proteomics 16, 2854-2863
- Akasaka-Manya, K., Manya, H., Sakurai, Y., Wojczyk, B. S., Kozutsumi, Y., Saito, Y., Taniguchi, N., Murayama, S., Spitalnik, S. L., and Endo, T. (2010) Protective effect of N-glycan bisecting GlcNAc residues on beta-amyloid production in Alzheimer's disease. Glycobiology 20, 99-106
- LaFerla, F. M., and Green, K. N. (2012) Animal models of Alzheimer disease. Cold Spring Harb Perspect Med 2
- Kizuka, Y., Kitazume, S., Fujinawa, R., Saito, T., Iwata, N., Saido, T. C., Nakano, M., Yamaguchi, Y., Hashimoto, Y., Staufenbiel, M., Hatsuta, H., Murayama, S., Manya, H., Endo, T., and Taniguchi, N. (2015) An aberrant sugar modification of BACE1 blocks its lysosomal targeting in Alzheimer's disease. EMBO Mol Med 7, 175-189
- Schedin-Weiss, S., Winblad, B., and Tjernberg, L. O. (2014) The role of protein glycosylation in Alzheimer disease. FEBS J 281, 46-62
- Das, U., Scott, D. A., Ganguly, A., Koo, E. H., Tang, Y., and Roy, S. (2013) Activity-induced convergence of APP and BACE-1 in acidic microdomains via an endocytosis-dependent pathway. Neuron 79, 447-460
- Toh, W. H., and Gleeson, P. A. (2016) Dysregulation of intracellular trafficking and endosomal sorting in Alzheimer's disease: controversies and unanswered questions. Biochem J 473, 1977-1993
- Schedin-Weiss, S., Gaunitz, S., Sui, P., Chen, Q., Haslam, S. M., Blennow, K., Winblad, B., Dell, A., and Tjernberg, L. O. (2020) Glycan biomarkers for Alzheimer disease correlate with T-tau and P-tau in cerebrospinal fluid in subjective cognitive impairment. FEBS J 287, 3221-3234
- Zhou, R. Z., Duell, F., Axenhus, M., Jonsson, L., Winblad, B., Tjernberg, L. O., and Schedin-Weiss, S. (2024) A glycan biomarker predicts cognitive decline in amyloid- and tau-negative patients. Brain Commun 6, fcae371
- Zhou, R. Z., Vetrano, D. L., Grande, G., Duell, F., Jonsson, L., Laukka, E. J., Fredolini, C., Winblad, B., Tjernberg, L., and Schedin-Weiss, S. (2023) A glycan epitope correlates with tau in serum and predicts progression to Alzheimer's disease in combination with APOE4 allele status. Alzheimers Dement 19, 3244-3249
- Hart, G. W. (2019) Nutrient regulation of signaling and transcription. J Biol Chem 294, 2211-2231
- Yuzwa, S. A., Shan, X., Macauley, M. S., Clark, T., Skorobogatko, Y., Vosseller, K., and Vocadlo, D. J. (2012) Increasing O-GlcNAc slows neurodegeneration and stabilizes tau against aggregation. Nat Chem Biol 8, 393-399
- Morris, M., Knudsen, G. M., Maeda, S., Trinidad, J. C., Ioanoviciu, A., Burlingame, A. L., and Mucke, L. (2015) Tau post-translational modifications in wild-type and human amyloid precursor protein transgenic mice. Nat Neurosci 18, 1183-1189
- Iqbal, K., Liu, F., and Gong, C. X. (2016) Tau and neurodegenerative disease: the story so far. Nat Rev Neurol 12, 15-27
- Hardiville, S., and Hart, G. W. (2014) Nutrient regulation of signaling, transcription, and cell physiology by O-GlcNAcylation. Cell Metab 20, 208-213
- Hastings, N. B., Wang, X., Song, L., Butts, B. D., Grotz, D., Hargreaves, R., Fred Hess, J., Hong, K. K., Huang, C. R., Hyde, L., Laverty, M., Lee, J., Levitan, D., Lu, S. X., Maguire, M., Mahadomrongkul, V., McEachern, E. J., Ouyang, X., Rosahl, T. W., Selnick, H., Stanton, M., Terracina, G., Vocadlo, D. J., Wang, G., Duffy, J. L., Parker, E. M., and Zhang, L. (2017) Inhibition of O-GlcNAcase leads to elevation of O-GlcNAc tau and reduction of tauopathy and cerebrospinal fluid tau in rTg4510 mice. Mol Neurodegener 12, 39
- Graham, D. L., Gray, A. J., Joyce, J. A., Yu, D., O'Moore, J., Carlson, G. A., Shearman, M. S., Dellovade, T. L., and Hering, H. (2014) Increased O-GlcNAcylation reduces pathological tau without affecting its normal phosphorylation in a mouse model of tauopathy. Neuropharmacology 79, 307-313
- Sato, Y., Naito, Y., Grundke-Iqbal, I., Iqbal, K., and Endo, T. (2001) Analysis of N-glycans of pathological tau: possible occurrence of aberrant processing of tau in Alzheimer's disease. FEBS Lett 496, 152-160
- Losev, Y., Frenkel-Pinter, M., Abu-Hussien, M., Viswanathan, G. K., Elyashiv-Revivo, D., Geries, R., Khalaila, I., Gazit, E., and Segal, D. (2021) Differential effects of putative N-glycosylation sites in human Tau on Alzheimer's disease-related neurodegeneration. Cell Mol Life Sci 78, 2231-2245
- Matsuzaki, K. (2020) Abeta-ganglioside interactions in the pathogenesis of Alzheimer's disease. Biochim Biophys Acta Biomembr, 183233
- Yanagisawa, K. (2015) GM1 ganglioside and Alzheimer's disease. Glycoconj J 32, 87-91
- Magistretti, P. J., Geisler, F. H., Schneider, J. S., Li, P. A., Fiumelli, H., and Sipione, S. (2019) Gangliosides: Treatment Avenues in Neurodegenerative Disease. Front Neurol 10, 859
- Yanagisawa, K., Odaka, A., Suzuki, N., and Ihara, Y. (1995) GM1 ganglioside-bound amyloid beta-protein (A beta): a possible form of preamyloid in Alzheimer's disease. Nat Med 1, 1062-1066
- Kakio, A., Nishimoto, S. I., Yanagisawa, K., Kozutsumi, Y., and Matsuzaki, K. (2001) Cholesterol-dependent formation of GM1 ganglioside-bound amyloid beta-protein, an endogenous seed for Alzheimer amyloid. J Biol Chem 276, 24985-24990
- Okada, T., Ikeda, K., Wakabayashi, M., Ogawa, M., and Matsuzaki, K. (2008) Formation of toxic Abeta(1-40) fibrils on GM1 ganglioside-containing membranes mimicking lipid rafts: polymorphisms in Abeta(1-40) fibrils. J Mol Biol 382, 1066-1074
- Utsumi, M., Yamaguchi, Y., Sasakawa, H., Yamamoto, N., Yanagisawa, K., and Kato, K. (2009) Up-and-down topological mode of amyloid beta-peptide lying on hydrophilic/hydrophobic interface of ganglioside clusters. Glycoconj J 26, 999-1006
- Itoh, S. G., Yagi-Utsumi, M., Kato, K., and Okumura, H. (2019) Effects of a Hydrophilic/Hydrophobic Interface on Amyloid-beta Peptides Studied by Molecular Dynamics Simulations and NMR Experiments. J Phys Chem B 123, 160-169
- Yamamoto, N., Yokoseki, T., Shibata, M., Yamaguchi, H., and Yanagisawa, K. (2005) Suppression of Abeta deposition in brain by peripheral administration of Fab fragments of anti-seed antibody. Biochem Biophys Res Commun 335, 45-47
- Hong, S., Ostaszewski, B. L., Yang, T., O'Malley, T. T., Jin, M., Yanagisawa, K., Li, S., Bartels, T., and Selkoe, D. J. (2014) Soluble Abeta oligomers are rapidly sequestered from brain ISF in vivo and bind GM1 ganglioside on cellular membranes. Neuron 82, 308-319
- Knight, E. M., Williams, H. N., Stevens, A. C., Kim, S. H., Kottwitz, J. C., Morant, A. D., Steele, J. W., Klein, W. L., Yanagisawa, K., Boyd, R. E., Lockhart, D. J., Sjoberg, E. R., Ehrlich, M. E., Wustman, B. A., and Gandy, S. (2015) Evidence that small molecule enhancement of beta-hexosaminidase activity corrects the behavioral phenotype in Dutch APP(E693Q) mice through reduction of ganglioside-bound Abeta. Mol Psychiatry 20, 109-117
- Oikawa, N., Yamaguchi, H., Ogino, K., Taki, T., Yuyama, K., Yamamoto, N., Shin, R. W., Furukawa, K., and Yanagisawa, K. (2009) Gangliosides determine the amyloid pathology of Alzheimer's disease. Neuroreport 20, 1043-1046
- Yamaguchi, T., Yamauchi, Y., Furukawa, K., Ohmi, Y., Ohkawa, Y., Zhang, Q., Okajima, T., and Furukawa, K. (2016) Expression of B4GALNT1, an essential glycosyltransferase for the synthesis of complex gangliosides, suppresses BACE1 degradation and modulates APP processing. Sci Rep 6, 34505
- Dukhinova, M., Veremeyko, T., Yung, A. W. Y., Kuznetsova, I. S., Lau, T. Y. B., Kopeikina, E., Chan, A. M. L., and Ponomarev, E. D. (2019) Fresh evidence for major brain gangliosides as a target for the treatment of Alzheimer's disease. Neurobiol Aging 77, 128-143
- Brinkmalm, G., Portelius, E., Ohrfelt, A., Mattsson, N., Persson, R., Gustavsson, M. K., Vite, C. H., Gobom, J., Mansson, J. E., Nilsson, J., Halim, A., Larson, G., Ruetschi, U., Zetterberg, H., Blennow, K., and Brinkmalm, A. (2012) An online nano-LC-ESI-FTICR-MS method for comprehensive characterization of endogenous fragments from amyloid beta and amyloid precursor protein in human and cat cerebrospinal fluid. J Mass Spectrom 47, 591-603
- Halim, A., Brinkmalm, G., Ruetschi, U., Westman-Brinkmalm, A., Portelius, E., Zetterberg, H., Blennow, K., Larson, G., and Nilsson, J. (2011) Site-specific characterization of threonine, serine, and tyrosine glycosylations of amyloid precursor protein/amyloid beta-peptides in human cerebrospinal fluid. Proc Natl Acad Sci U S A 108, 11848-11853
- Bennett, E. P., Mandel, U., Clausen, H., Gerken, T. A., Fritz, T. A., and Tabak, L. A. (2012) Control of mucin-type O-glycosylation: a classification of the polypeptide GalNAc-transferase gene family. Glycobiology 22, 736-756
- Akasaka-Manya, K., Kawamura, M., Tsumoto, H., Saito, Y., Tachida, Y., Kitazume, S., Hatsuta, H., Miura, Y., Hisanaga, S. I., Murayama, S., Hashimoto, Y., Manya, H., and Endo, T. (2017) Excess APP O-glycosylation by GalNAc-T6 decreases Abeta production. J Biochem 161, 99-111
- Kitazume, S., Tachida, Y., Kato, M., Yamaguchi, Y., Honda, T., Hashimoto, Y., Wada, Y., Saito, T., Iwata, N., Saido, T., and Taniguchi, N. (2010) Brain endothelial cells produce amyloid {beta} from amyloid precursor protein 770 and preferentially secrete the O-glycosylated form. J Biol Chem 285, 40097-40103
- Tachida, Y., Iijima, J., Takahashi, K., Suzuki, H., Kizuka, Y., Yamaguchi, Y., Tanaka, K., Nakano, M., Takakura, D., Kawasaki, N., Saito, Y., Manya, H., Endo, T., and Kitazume, S. (2023) O-GalNAc glycosylation determines intracellular trafficking of APP and Abeta production. J Biol Chem 299, 104905
- Greenberg, S. M., Gurol, M. E., Rosand, J., and Smith, E. E. (2004) Amyloid angiopathy-related vascular cognitive impairment. Stroke 35, 2616-2619
- Jonsson, T., Stefansson, H., Steinberg, S., Jonsdottir, I., Jonsson, P. V., Snaedal, J., Bjornsson, S., Huttenlocher, J., Levey, A. I., Lah, J. J., Rujescu, D., Hampel, H., Giegling, I., Andreassen, O. A., Engedal, K., Ulstein, I., Djurovic, S., Ibrahim-Verbaas, C., Hofman, A., Ikram, M. A., van Duijn, C. M., Thorsteinsdottir, U., Kong, A., and Stefansson, K. (2013) Variant of TREM2 associated with the risk of Alzheimer's disease. N Engl J Med 368, 107-116
- Colonna, M., and Wang, Y. (2016) TREM2 variants: new keys to decipher Alzheimer disease pathogenesis. Nat Rev Neurosci 17, 201-207
- Melchior, B., Garcia, A. E., Hsiung, B. K., Lo, K. M., Doose, J. M., Thrash, J. C., Stalder, A. K., Staufenbiel, M., Neumann, H., and Carson, M. J. (2010) Dual induction of TREM2 and tolerance-related transcript, Tmem176b, in amyloid transgenic mice: implications for vaccine-based therapies for Alzheimer's disease. ASN Neuro 2, e00037
- Guerreiro, R., Wojtas, A., Bras, J., Carrasquillo, M., Rogaeva, E., Majounie, E., Cruchaga, C., Sassi, C., Kauwe, J. S., Younkin, S., Hazrati, L., Collinge, J., Pocock, J., Lashley, T., Williams, J., Lambert, J. C., Amouyel, P., Goate, A., Rademakers, R., Morgan, K., Powell, J., St George-Hyslop, P., Singleton, A., Hardy, J., and Alzheimer Genetic Analysis, G. (2013) TREM2 variants in Alzheimer's disease. N Engl J Med 368, 117-127
- Atagi, Y., Liu, C. C., Painter, M. M., Chen, X. F., Verbeeck, C., Zheng, H., Li, X., Rademakers, R., Kang, S. S., Xu, H., Younkin, S., Das, P., Fryer, J. D., and Bu, G. (2015) Apolipoprotein E Is a Ligand for Triggering Receptor Expressed on Myeloid Cells 2 (TREM2). J Biol Chem 290, 26043-26050
- Park, J. S., Ji, I. J., Kim, D. H., An, H. J., and Yoon, S. Y. (2016) The Alzheimer's Disease-Associated R47H Variant of TREM2 Has an Altered Glycosylation Pattern and Protein Stability. Front Neurosci 10, 618
- Sun, R. C., Young, L. E. A., Bruntz, R. C., Markussen, K. H., Zhou, Z., Conroy, L. R., Hawkinson, T. R., Clarke, H. A., Stanback, A. E., Macedo, J. K. A., Emanuelle, S., Brewer, M. K., Rondon, A. L., Mestas, A., Sanders, W. C., Mahalingan, K. K., Tang, B., Chikwana, V. M., Segvich, D. M., Contreras, C. J., Allenger, E. J., Brainson, C. F., Johnson, L. A., Taylor, R. E., Armstrong, D. D., Shaffer, R., Waechter, C. J., Vander Kooi, C. W., DePaoli-Roach, A. A., Roach, P. J., Hurley, T. D., Drake, R. R., and Gentry, M. S. (2021) Brain glycogen serves as a critical glucosamine cache required for protein glycosylation. Cell Metab 33, 1404-1417 e1409

