
氏名:宮川 淳
名古屋工業大学大学院工学研究科工学専攻生命・物質化学プログラム 准教授
2001年に埼玉大学工学部機能材料工学科を卒業し、2006年に東京大学大学院工学系研究科化学生命工学専攻博士後期課程を修了し、博士(工学)を取得(指導教員:畑中研一教授)。その後、理化学研究所伊藤細胞制御化学研究室の協力研究員、2009年から名古屋工業大学大学院工学研究科 助教となり、2019年から現職。
多糖は、単糖が多数連結した構造をしており、糖の間は1種類または複数種類の結合様式で連続して連結している。これらの多糖は、エネルギー源として貯蔵されるものや細胞壁の構成要素として構造材料となるだけでなく、生理活性分子として多様な生体制御機能を示すものが知られている。しかし、その構造の複雑さゆえに、多糖の詳細な機能解明は困難であり、化学合成により構築された部分構造を用いた機能解明が進められてきた。その中で、糖鎖高分子を利用して単糖やオリゴ糖を系統的に配置し、多糖に類似した構造を模倣する試みがなされている。
本稿では、多糖の中でも古くから免疫活性化能を知られ、医薬品としても利用されてきたβグルカンを解説する。特に、βグルカンの化学合成法および高分子化による模倣分子の構築手法について、我々の研究成果を中心に紹介する。
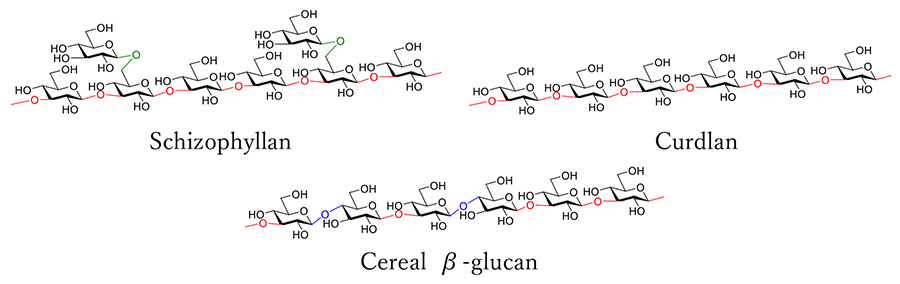
βグルカンは、グルコースがβ1,3結合で繰り返し結合した多糖類の総称である。その中には、グルコースがβ1,6結合した分岐鎖をもつものや、β1,4結合を主鎖にもつものも含まれる(図 1)1-3。βグルカンは、細菌、真菌、藻類、植物など多様な生物群に広く存在し、細胞壁の主要構成要素や栄養源として機能する。特に真菌類であるキノコの細胞壁の構成成分であるβグルカンの中でも、シイタケ由来のレンチナン(Lentinan)および霊芝由来のシゾフィラン(Schizophyllan)が注目されており、抗腫瘍免疫活性化作用がある薬剤として利用されてきた。一方、分岐鎖をもたないβ1,3結合のみで構成されるカードラン(Curdlan)は非水溶性であり、その立体構造やゲル化特性が研究されている4。また主鎖にβ1,4結合をもつβグルカンは、大麦やオーツ麦などの穀草類に多く含まれ、これらも免疫活性化作用を示すことが報告されている。さらに、βグルカンは抗感染作用、抗酸化作用、腸内環境の改善、血糖値の調整、コレステロール濃度の調整、抗炎症作用など、幅広く生理機能をもつことが知られている5-7。
βグルカンの特徴的な立体構造として、三重らせん構造が知られている。また、凝集した粒子状構造やランダムコイル構造も存在することが報告されている8,9。三重らせん構造は、分子内および分子間の水素結合によって安定化されており、この水素結合は強アルカリ性水溶液中やジメチルスルホキシド中では切断され、構造がほどけて単鎖のランダムコイル構造に変化する。一方、疎水性の高いβグルカンは水への溶解性が低く、分子が凝集した粒子状の構造を形成する。この粒子状構造は、健康食品として市販されているβグルカンに多くみられる。これらの中でも特に三重らせん構造は注目されており、DNAや疎水性化合物(葉酸やポリフェノールなど)との複合体を形成して輸送体としての利用が研究されている。またその三重らせん構造が免疫活性化作用を生み出す原因として考えられていた10。一方、粒子状のβグルカンの研究も進んでおり、免疫活性化作用があることが報告されている11。また分子量が約100万もあるβグルカンは、免疫活性化作用を示すが、分子量が数千程度になると免疫受容体に対するアンタゴニストとなり、免疫活性化を抑制することが報告され、免疫活性化には分子量が重要であることがわかる12。
βグルカンの立体構造による免疫活性化作用は依然として不明確であり、それぞれの構造特性における活性は、個別に研究が行われており、それらを単純に比較することは困難である。

βグルカンの生産方法として菌類や酵素を利用した手法についての詳細は、既報の総説を参照されたい13,14。本稿では、主に2019年以降の化学合成法に基づく最新の研究について述べ、それ以前の研究に関しては総説に記載されている15。
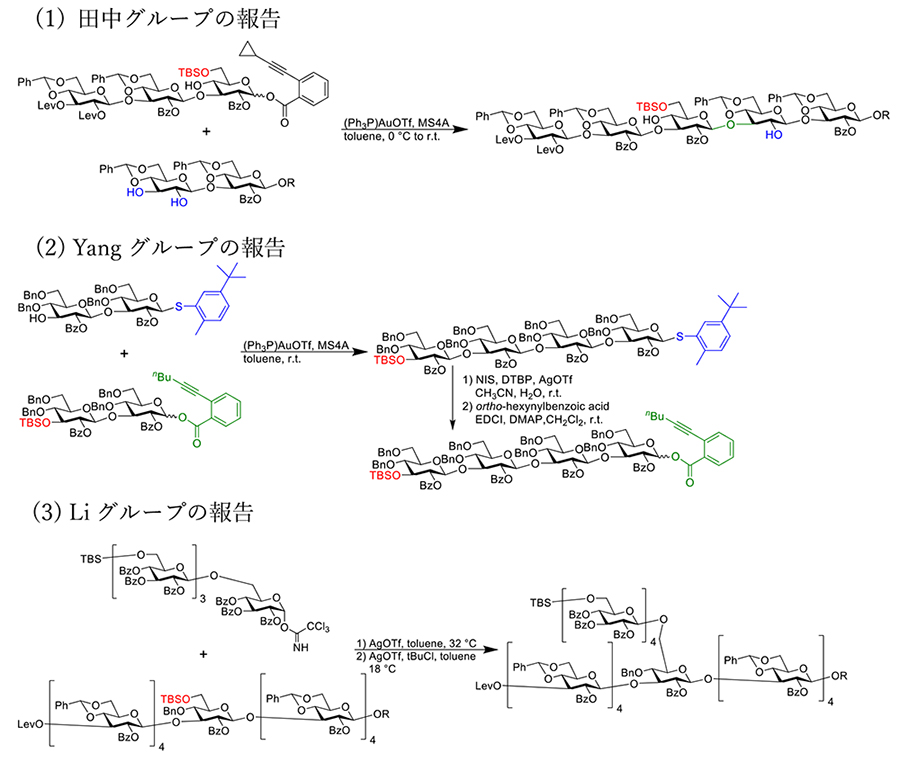
田中らのグループによる研究では、シゾフィラン型のβグルカン14糖の合成を報告している16。 この合成は、筆者らが以前に行った研究に基づき、糖受容体の2,3-位水酸基を無保護の状態で位置選択的にグリコシル化する手法を用いている(図 3 (1))。3糖ビルディングブロックを用いて連結反応を行い、酸に不安定なベンジリデン基を含むため、穏和な金触媒を用いたグリコシル化を利用している。分岐鎖の導入については、ベンジリデン基を還元開裂してシリル保護基の導入を行った後、主鎖の構築を完了した段階で一括して導入する手法を採用している。Yangらのグループは、ベンジル保護基を4,6位に導入したアームド受容体およびアームド供与体を用いて合成を進めた(図 3 (2))。供与体の1位の活性化基にはアルキニルベンゾエートを使用し、受容体の1位保護基には立体的に嵩高い5-tert-ブチル-2-メチルベンゼンチオールを選択することで、グリコシル化後にチオグリコシドをアルキニルベンゾエートに付け替え、供与体へと変換可能にした。この手法を活用し、コンバージェント合成による直鎖16糖のβグルカン合成を達成している17。さらにLiらのグループは、主鎖として4糖ブロックを合成後、分岐鎖用の単糖を連結し、4糖ブロックで挟む形で合成を行った(図 3 (3))。その後、分岐鎖としてβ-1,6結合で連結した4糖ブロックを導入し、分岐鎖が4糖、直鎖が9糖のβグルカンの合成を達成している18。
β-1,3-結合の構築において、多くの研究者が4,6-ベンジリデン保護基を使用し、2位水酸基にはβ選択性を向上させるためアセチル基またはベンゾイル基を用いている。一方で、3位水酸基の反応性を適切に制御するためには保護基の選択が重要であり、4位水酸基による3位水酸基への立体障害を低くすることやアームド保護基を使用することが必要である。特にベンジリデン基は、水酸基の自由度を下げる架橋型の保護基であるため、有効である。しかし、分岐鎖を導入するためにはベンジリデン基のままでは困難であるため還元開裂を行い、4位ベンジル基および6位無保護水酸基という形に変換し、6位にシリルやカーボネート基の選択的に脱保護可能な官能基を導入する必要がある。
我々のグループでは、分岐鎖導入のためにベンジリデン基を用いず、還元開裂させた供与体および受容体を合成した19。この手法では分岐鎖を導入するユニットとして、6位にクロロアセチル基を用い、アセチル基をもつユニットと区別して合成した。その後、クロロアセチル基とアセチル基をもつユニットの配置を変え、主鎖3糖を合成した後にクロロアセチル基を選択的に除去し、分岐鎖を導入位置が異なる分岐オリゴ糖を合成した。その過程を通じて、中央に分岐鎖を有するβグルカン4糖オリゴ糖を用いたシゾフィランの模倣体を作る計画を立てた。
糖認識タンパク質と糖分子間の弱い相互作用を高めるため、糖を集積化する高分子化が有効な手法として用いられてきた。糖認識タンパク質が複数の糖結合サイトを有する場合、複数の糖が同時に結合することでクラスター効果が発揮され、相互作用の親和性が向上することが知られている20–22。特に植物レクチンや細菌毒素に対する高親和性高分子の研究が多く行われ、その有効性が実証されている。
しかし、多糖とその認識タンパク質との結合を模倣する研究例は限られている。これは多糖が認識される部分構造を合成することが困難であることに加え、その糖ユニットを高分子化する工程がさらに困難であるためである。アミノ基や硫酸基、カルボキシ基などのイオン性官能基を有する多糖については、これらのイオン結合を再現することで強い相互作用をもつ高分子が合成されている。多糖の繰り返し構造に含まれる二糖や単糖ユニットを用いて重合し、繰り返し構造を模倣することで、強い相互作用を実現する試みが報告されている23,24。
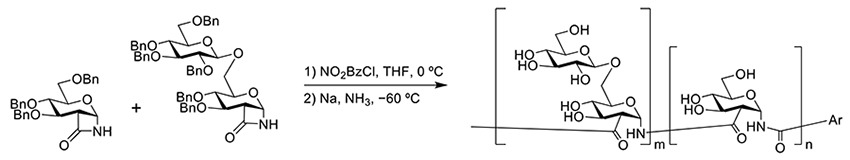
また、イオン性官能基をもたない中性多糖では、模倣分子の研究は限られている。その中でもβグルカン模倣高分子の例として、最近報告されたものがある。Grinstaffらのグループによる報告では、グルコースラクタムとゲンチビオースラクタムを用いた開環重合によりβグルカン模倣高分子を合成している(図 4)25。主鎖はアミド結合で連結しており、β1,3結合はもたないが、グルコースが連続して並んでおり、ゲンチビオース由来の分岐鎖様のβ1,6結合のグルコースをもつ分子である。またこの模倣分子は水溶液中でα-ヘリックス構造をとっていることもCDスペクトルから確認している。この模倣分子の生物活性は、Dectin-1を介した免疫活性化能を示すことが報告されており、30%程のゲンチビオース含有高分子が最も高い活性を示し、分子量は大きくなるにつれて、活性が上昇した。この模倣分子は、βグルカンの立体構造を模倣しており、そのヘリックス構造から外側にβ1,6結合したグルコースが露出していることが考えられ、分岐鎖の重要性を示している。
一方、我々は中性多糖であるβグルカンのリガンドを集積化した模倣する高分子の合成に挑戦した。βグルカンがその受容体であるDectin-1に認識される糖残基の数は、10糖程度必要であるとする研究や、3糖や6糖など少ない残基数でも結合するとする研究が報告されている26–28。
そこでDectin-1に結合する最小単位が直鎖3糖であるという報告と、分岐鎖を有するβグルカンの免疫活性化能が高いとの知見を統合し、先ほど合成を示した直鎖3糖の真ん中に分岐鎖1糖をもつ4糖オリゴ糖をDectin-1に結合する最小単位として設計した。またβグルカンは溶液中で多様な立体構造をとることが知られているため、重合後に高分子骨格を修飾し、異なる物性を有する高分子を調整することを計画した。
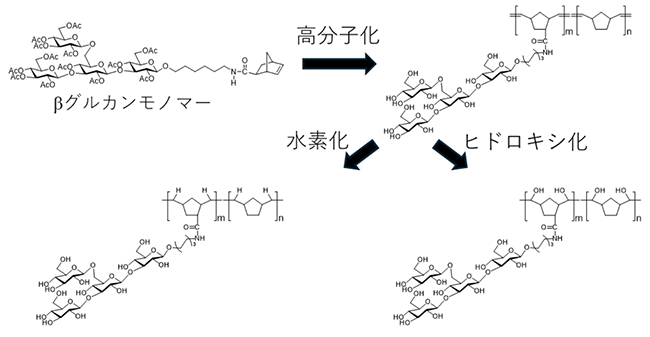
具体的には、疎水的なβグルカンを模倣するため、主鎖に疎水的な骨格であるノルボルネンを用いて重合を行い、βグルカン4糖を有する高分子を合成した。また分岐鎖の有無について比較するため、βグルカン直鎖3糖を有する高分子も同時に合成し、さらに糖密度の異なる高分子の合成も行った。その後、重合過程で生じる二重結合に対し、水素化およびヒドロキシ化を行い、高分子骨格を修飾した(図 5)。
これにより、分子量や分子量分布が同一であるが、主鎖構造が異なる高分子を調製し、βグルカン模倣高分子ライブラリーを構築した。そのライブラリーは、高分子中の糖鎖構造、糖含有量、および主鎖骨格の多様性を有しており、糖認識タンパク質との相互作用を詳細に検討するための有用なツールとなり得る。
これまでに化学合成された天然型のβグルカンを用いたDectin-1との結合評価および免疫活性化評価に関する田中らの報告によると、Dectin-1に結合可能な十分な鎖長を有するβグルカンであっても、必ずしも強い免疫応答を引き起こすわけではないことが示されている29。一方で、天然のβグルカンを用いた研究では、免疫活性化を実現するためには、多数のDectin-1を集積化する必要があることが報告されている30。これらの結果から、高分子量が免疫応答において重要であると考えられ、高分子を基盤としたアプローチを採用する計画へとつながった。
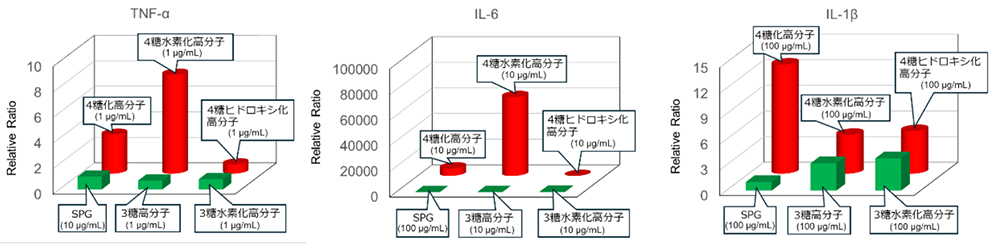
我々は、マウス由来のマクロファージRAW264細胞を用い、高分子ラブラリーの免疫活性化評価を実施した。図 6には免役応答の指標としてTNF-α、IL-1β、IL-6の生産量をELISA試験によって比較評価の結果として、特に活性が高かった糖とノルボルネンの比が1:3の高分子の結果をまとめた31。基準物質として天然のSchizophyllan(SPG)を用いた結果、分岐鎖を有する4糖をもつ高分子、特に主鎖を未修飾または水素化された高分子が極めて高い活性を示した。一方、類似した構造を有する主鎖3糖を含む高分子は、SPGと類似した活性を示した。この結果から、免疫応答を強く引き起こすためには、分岐鎖を有する構造が重要であることが示された。また、主鎖骨格の疎水的も免疫活性化に寄与する要因として明らかになった。
すなわち、βグルカンの免疫活性化において、分岐鎖の存在が重要であること、ならびにβグルカンが有する疎水性がDectin-1との結合を介した免疫活性化に必要であることが明らかになった。これらの知見は、βグルカンの立体構造や物性が免疫応答の制御において、重要な役割を果たすことを示唆している。今後は、さらなる構造の最適化を通じて、より高い免疫活性化能を有する分子の設計を進めるとともに、誘導されるサイトカインの制御を目指していきたい。
本研究では、βグルカンという中性多糖の生物活性を模倣することを目指し、βグルカンオリゴ糖の合成、高分子化、および高分子修飾に関する複合的な検討を行った。βグルカンの免疫受容体としてDectin-1だけでなく、CR3など複数の受容体が存在するため、これらの詳細な相互作用の解明が今度の課題である。しかし、本研究で採用した手法は、糖鎖高分子を用いた多糖模倣技術の発展に寄与し、リガンドとなる糖鎖の構造および高分子主鎖の構造が免疫活性化において重要な役割を果たすことを再認識するものとなった。糖鎖高分子の設計においては、親水性骨格または疎水性骨格を選択して使用することがこれまで行われてきたが、どちらの設計が優れるかは、ターゲットとなるタンパク質との相互作用に依存することが示された。また、単にリガンド糖鎖を並べるだけでは最適な効果を得られないことも明らかになった。
今後、多糖を模倣する分子をより効率的に構築するためには、高分子化技術がますます重要となる。これらの技術のさらなる発展により、免疫応答の精密な制御や新規医薬品の開発に貢献できると期待される。