
氏名:長岡 清記
奈良先端科学技術大学院大学 先端科学技術研究科
2020年4月、奈良先端科学技術大学院大学、博士課程前期課程入学。2022年3月、同修了、修士(工学)

氏名:吉田 裕安材
奈良先端科学技術大学院大学 先端科学技術研究科
2011年、大阪大学大学院工学研究科修了(日本学術振興会DC1)。博士(工学)。2011年アメリカ合衆国ジョージア工科大学、博士研究員(日本学術振興会、海外特別研究員)。2013年10月、大阪大学大学院、博士研究員。2014年9月、信州大学学術研究院、助教。2019年4月、信州大学先鋭領域融合研究群先鋭材料研究所、助教(兼任)。2019年11月、奈良先端科学技術大学院大学、助教

氏名:網代 広治
奈良先端科学技術大学院大学 先端科学技術研究科、データ駆動型サイエンス創造センター、メディルクス研究センター
2004年名古屋大学大学院工学研究科修了(日本学術振興会DC2)。博士(工学)。2004年アメリカ合衆国コーネル大学博士研究員(日本学術振興会、PD含む)。2006年大阪大学臨床医工学融合研究教育センター、特任講師。2011年、同特任准教授。2015年奈良先端科学技術大学院大学、物質創成科学領域、特任准教授。2019年4月、同教授。2024年7月、同大学メディルクス研究センター、研究推進部門長(兼任)
アガロース溶液のエレクトロスピニング法において、溶媒条件を探索・最適化したところ、ヘキサフルオロイソプロパノール/水 (92.5/7.5、v/v)の条件下で直径68 ± 33 nmのナノファイバーを調製することができた。この結果は、アガロース材料をナノスケールで材料化する場合には、溶媒の水素結合制御が重要であることを示唆している。
近年、持続可能な開発目標(SDGs)の達成に向けた取り組みや、石油由来材料の代替として天然化合物の活用が大きな注目を集めている。これらの動向は、天然化合物に関する研究課題が新たな技術革新の分野において、重要であることを示している。
アガロース1–3は天然由来の高分子で、高温で水に溶解し冷却するとゲル化する。このゲル化現象は、弱い分子間水素結合によるものであり、再加熱によって結合が解離し、溶液中で構造が復元すると考えられているが4、この機構は未だ明らかとされていない。高い安全性が期待されるアガロース材料は電気泳動技術や生医学材料分野で広く応用されているが5、その独自の性質は汎用性・加工性を大きく制限していると言える。これに対して、アガロースのブレンド材料の検討も進められ、例えばキトサンとのブレンドによるハイドロゲルやファイバー6、スポンジ状材料7、マイクロカプセル8など、様々な形状の材料開発が報告されている。以上のことから、アガロースの効果的な水素結合は系全体を固化するバルク材料の作製には有用であるが、特にナノサイズなど微細な構造の作製には不向きであり、これまで十分に探求されていない。つまり、現在のところ純粋なアガロースのみを用いたナノ材料の実例は確認されていない。
エレクトロスピニングは、高分子溶液に正の高電圧を印加し、液滴内で静電反発を誘導した後、通常負に帯電したコレクターに溶液を噴霧するプロセスである。目的とする繊維形態を得るためには、最適な条件の特定が重要である9。さらに、ビーズの発生が繊維構造の物理的特性に影響を与えることが報告されている10。ビーズ形成は、低表面張力、高濃度溶液、ポリマーの分子量によって制御可能であるが、繊維の直径が大きくなる可能性がある11。湿度によるビーズ形成の制御も示されており、これにより直径が小さく、ビーズのない繊維が生成されることが報告されている12。ナノスケールの繊維は、マイクロスケールの繊維に比べて表面積が飛躍的に増大し、何千倍もの表面積を有することができる。これにより、不織布を貫通する分子や粒子との効率的な接触が可能となる13,14。エレクトロスピニングは、石油由来の高分子15、デキストラン16、セルロース17、アルギン酸18など、さまざまな材料で報告されているが、アガロースを用いたエレクトロスピニングの例は極めて限定的である。
アガロースのエレクトロスピニングに関しては、カルボキシル化アガロース19やアセチル化アガロース20、さらにはアガロースとキトサン5、ポリアクリル酸21、ポリアクリルアミド22、ポリビニルアルコール23、アルギン酸24、およびクルドラン25のブレンド溶液で報告されている。しかし、私たちの知る限り、純粋なアガロースのみを用いたエレクトロスピニングの成功例は見当たらない。湿式紡糸によって、直径約120 μmのアガロース繊維作製が1例のみ報告されているが26、ナノサイズには達していないのが現状であった。 本研究では、エレクトロスピニングを用いてナノスケールのアガロース繊維を得ることを目的とした。このため、溶媒の検討、添加剤の使用、温度や針の長さの変化を適用し、分子間水素結合の相互作用を制御する条件を設定した(図 1)。

表1に、さまざまな溶媒および添加剤を使用したアガロース溶液のエレクトロスピニング条件をまとめた。また図 2に、レーザー顕微鏡で観察された結果の外観を示す。アガロースのエレクトロスピニングを実現するためには、分子内水素結合を解き、溶媒化する必要がある。そこで水素結合を制御することを目的としてシリンジにヒーターを装着し、通常使用される3.7 cmの針ではなく、1.2 cmの短いピッチの針を用いた。まず、トリフルオロ酢酸(TFA)とジクロロメタン(DCM)を7/3(v/v)の比率で混合し(表 1、entry 1)、キトサンとアガロースの混合物で得られた条件を参考にしたが5、観察されたのは粒子のみであった(図 2a)。次に水系の溶液条件を検討し、エタノールおよびヘキサフルオロイソプロパノール(HFIP)を用いて、水と添加剤を混合した溶媒を選択した。

クエン酸およびグルコースは、水およびエタノール中の添加剤として使用され、これらの添加剤は室温でのゲル化を防ぐ役割を果たす(表 1、entries 2–4)。しかし、水/エタノール(3/2、v/v)に0.5 wt%のグルコースを添加した場合、観察されたのはレンズ型の形状のみであった(図 2b)。溶液中に添加剤が存在すると、操作後も放電側からスピニングされるアガロースに添加剤が残留するため、分子間水素結合の制御が困難になる可能性がある。そのため、スピニング過程で除去可能な低沸点の揮発性溶媒を使用した。この場合、室温でのゲル化を防ぐためにシリンジを加熱し、短い繊維が形成された(表 1、entries 5, 6)。水/エタノール(3/2、v/v)中2.0 wt%の条件では、繊維の直径は1.30 ± 0.37 μmと推定された(図 2c)。しかし、繊維の形成はこの条件下でのみ確認され、再現性が低く、他のサンプルはすべて失敗に終わった。シート型ヒーターでシリンジを加熱した場合、針先でのゲル化がほとんどのサンプルで観察され、即時の注入が実質的に不可能であった。また、過熱はエタノール溶媒の蒸発を引き起こし、制御を複雑化させた。このシステムでは、シート型ヒーターをエレクトロスピニング装置の密閉空間に配置して電流を流して加熱すると、端子が近接しているために電場干渉が生じ、装置エラーが発生した。したがって、次に、加熱せずにアガロースの分子内水素結合を解き、溶媒化するために、HFIPを溶媒として選択した。
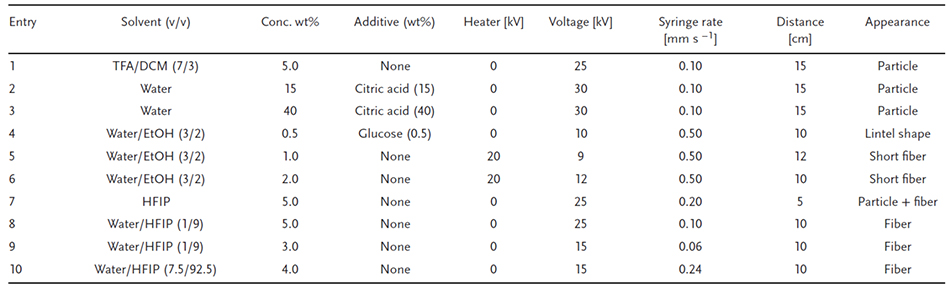
HFIP中で5.0 wt%のアガロースを使用した場合、少量の繊維と粒子が観察された(表 1、entry 7)。続いてアガロース内の水素結合の相互作用を変えるため、HFIPに水を混合し、その後スピニング条件を調整した。水/HFIP(1/9、v/v)を使用し、シリンジの流速を0.10 mm s−1に設定し、10 cmの距離でスピニングを行った場合(表 1、entry 8)、HFIP溶媒のみを使用した場合に比べて繊維の量が増加した(図 2d)。さらに、15 kVでシリンジの流速を0.06 mm s−1に遅くし、3.0 wt%に希釈した水/HFIPを使用した場合(表 1、entry 9)、明らかに透明な繊維が観察された(図 2e)。ここで、アガロース溶液の粘度が繊維形成に大きく寄与していると仮定し、水とHFIPの比率およびアガロース濃度を変化させた際の粘度の関係を測定したところ、アガロースの全ての濃度(1.5、2.0、2.5、3.0 wt%)において、水/HFIP溶媒中における水7.5 vol%で、最も高い粘度が5 vol%から10 vol%の範囲で観察された。さらに、水の濃度が5 vol%以下および10 vol%以上では、アガロースの溶解性が低下した。最終的に、水/HFIP(7.5/92.5、v/v)中で4.0 wt%を使用したところ(表 1、entry 10)、非常に明瞭な繊維が観察された(図 2f)。
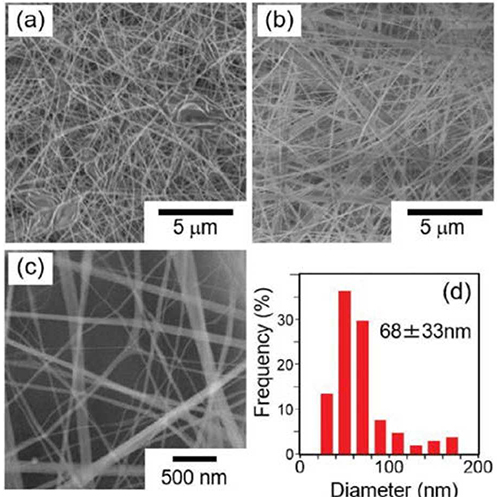
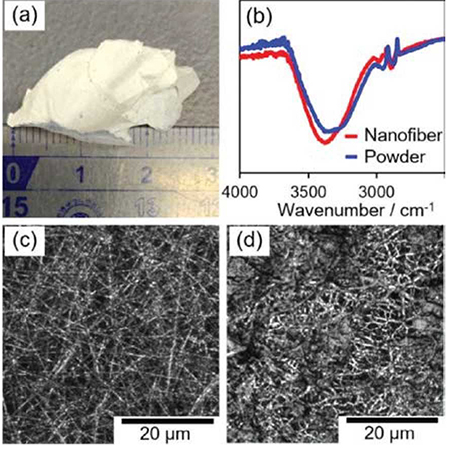
アガロースナノファイバーを高解像度の電界放出型走査電子顕微鏡(FE-SEM)で観察した。アガロースナノファイバーをHFIPのみで作製した場合、いくつかの領域で構造が崩れたように見える大きな粒子が形成され、繊維が一体化している様子が観察された(図 3a)。しかし、水/HFIP(7.5/92.5、v/v)中で4.0 wt%の高粘度溶媒を使用した場合には、状態の良い繊維が確認された(図 3b)。高倍率で観察すると、繊維の表面が滑らかであることがより明確に確認された(図 3c)。繊維の直径は画像から測定され、結果を棒グラフとして比較したところ、繊維の直径は68 ± 33 nmと推定され、これは以前報告されたアガロース繊維の直径120 μm26の約1/1200に相当し、新規で極めて細かい材料が得られたことを示している。驚くべきことに、ナノファイバーを積層させることで、ナノファイバーシートの作製が可能であった(図 4a)。
アガロースナノファイバーの特性を調べるために、3500~3000 cm−1の範囲で水素結合領域のフーリエ変換赤外分光法(FT-IR)スペクトルをアガロース粉末と比較した(図 4b)。その結果、アガロースナノファイバー中のヒドロキシ基の伸縮振動のピークトップが、より高い波数領域にシフトしていることが観察された(図 4b)。これは、アガロースナノファイバーにおける水素分子の結合がアガロース粉末よりも少ないことを示唆している。材料の安定性を確保するためには、未形成の水素結合を減らす必要があるかもしれない。湿潤環境下で高温加熱することでアガロースを熱架橋しようと試みたが、FT-IR測定ではヒドロキシ基のピークに変化は見られなかった。水素結合中の未形成ヒドロキシ基を減らすことは今後の課題である。
最後に、アガロースナノファイバーのゲルファイバーとしての膨潤率(S.R.)を推定した。S.R.は以下の式(式A)で定義され、ここでwsは高湿度条件下での平衡膨潤ファイバーの重量を表し、25℃の密閉容器内で十分な量の水を用いて飽和湿度に達した状態を意味する。wdは乾燥ファイバーの重量である。S.R.は約15であり、一般的なバルクアガロースゲルよりも低かったが、中性ハイドロゲルが示す膨潤度とほぼ同等か、それ以上の膨潤度を示した。
S.R. = (ws - wd)/wd (A)
エレクトロスピニングを用いてアガロースナノファイバーを作製する方法を開発した。繊維の直径は68 ± 33 nmで、従来報告されているものよりもはるかに細かった。作製時には水素結合の制御および低沸点溶媒の使用が重要であると考えられる。この新規アガロースファイバーは、天然由来の材料によって得られる大きな表面積を活かし、今後さまざまな応用が期待される。