
氏名:杉浦 信夫
本著者・杉浦は生化学者であり,この十年間は酵素化学的方法を用いた人工コンドロイチン硫酸ライブラリーの構築と,その合成多糖体と生理活性分子群との相互作用について研究している。彼は1976年名古屋大学理学部化学科で学士を取り,1995年に静岡県立大学薬学部にて薬学博士を取得した。博士論文はグリコサミノグリカン-脂質誘導体の合成と生物活性に焦点を当てた研究であった。名古屋大学では鈴木旺教授の研究室で学び,大学卒業後,天野エンザイム株式会社に入社し放線菌ヒアルロニダーゼなどの細菌酵素やバイオリアクターの研究,および静岡県立大学・矢内原昇教授の研究室で硫酸化ペプチドホルモンであるコレシストキニンなどの脳−腸管ペプチドの研究に携わってきた。その後,1988年に生化学工業株式会社に入社し,愛知医科大学・分子医科学研究所の木全弘治教授のもとでグリコサミノグリカンの化学修飾と生物活性に関する研究をしてきた。2007年に愛知医科大学・同研究所の准教授に就任し(渡辺秀人教授),合成ライブラリーと関連酵素を用いたグリコサミノグリカンの生物機能の研究を行い現在に至っている。
コンドロイチン硫酸(CS)はグリコサミノグリカン(GAG)ファミリーの一員であり,直鎖多糖体構造であり,プロテオグリカンの形態で細胞外マトリックスや細胞表面に普遍的に分布している1。脊椎動物のCSプロテオグリカンは軟骨,腱,靱帯,動脈,および脳に豊富に存在し,発生,器官形成,炎症および感染などにおいて重要な生物機能を担っている。脊椎動物だけでなく,無脊椎動物,例えば線形動物(線虫)2,棘皮動物(ウニ)3,軟体動物(イカ)4,および節足動物(昆虫)5, 6など,多くの動物種がCSプロテオグリカンを産生する。
プロテオグリカン中のCS鎖はそのコアタンパク質のセリン残基に結合四糖を介して共有結合している。CS骨格であるコンドロイチン鎖はN-アセチル-D-ガラクトサミン(GalNAc)とD-グルクロン酸(GlcA)とが交互に繰り返し結合することで多糖体を形成している。高分子形成の過程で,糖鎖は各種硫酸基転移酵素によって様々な位置に硫酸基の修飾を受ける7。主要なCS構造単位は未硫酸化二糖(0S, GlcA-GalNAc),GalNAc残基C-4位1硫酸化二糖(4S, GlcA-GalNAc4S),GalNAc残基C-6位1硫酸化二糖(6S, GlcA-GalNAc6S)の3種である(Fig.1)。
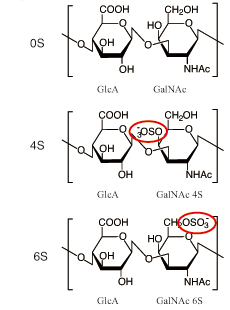
Fig. 1 主要な3種CS二糖単位の構造式
0S; 無硫酸化糖,4S; GalNAc残基4位単硫酸化二糖,6S; GalNAc残基6位単硫酸化二糖
さらに多硫酸化されたdiSD (GlcA2S-GalNAc6S), diSE (GlcA-GalNAc4S6S), および triS (GlcA2S-GalNAc4S6S)構造もCS二糖単位として存在する。CS鎖の生物機能は主にその硫酸基と構造特異性および多糖体骨格の多様性に依存している。
CS鎖を開裂するコンドロイチナーゼ(コンドロイチンリアーゼ)はProteus vulgaris8,Flavabacterium heparinum9,およびArthrobactor aurescens10などの細菌が産生することが知られている。GalNAcとGlcA残基間のグリコシド結合を開裂し,その際に232 nmの紫外線吸収をもつ4,5−不飽和ウロン酸残基を生み出すことから11,CSの分析に広く用いられてきた。脊椎動物ではヒアルロニダーゼ1や4のような加水分解酵素がCSを分解すると報告されており,CSの代謝に寄与している12。その加水分解物は飽和オリゴ糖であり,232 nmの紫外線吸収は持たない。
最近,我々はコンドロイチン硫酸基転移酵素をバキュロウイルスの系で発現を試みたところ,バキュロウイルス感染昆虫細胞の培養液中にコンドロイチン分解活性が存在するのを見出した13。その培養液から活性分子を精製し,それがバキュロウイルスAuotgrapha californica nucleopolyhedrovirus (AcMNPV) の包埋体由来ウイルス(ODV)のエンベロープタンパク質の一つODV-E66のN-末端欠損分子であることを突き止めた。その後,バキュロウイルスBombyx mori nucleopolyhedrovirus (BmNPV) のゲノムからもODV-E66相同遺伝子をクローニングし,それら精製タンパク質及び発現組換えタンパク質の酵素学的な性質を調べた14。BmNPV由来のBmODV-E66は,AcMNPV由来のAcODV-E66に比べ,アミノ酸配列で92%の相同性があり,83%の酵素活性を示し,同一の基質特異性をもつなどの酵素特性を示した。さらに,BmNPVの宿主昆虫であるカイコ Bombyx mori の幼虫にCSが存在すること,並びにその組織分布を調べた14。これらの結果から、バキュロウイルスのコンドロイチナーゼ ODV-E66は宿主昆虫へのウイルス感染を促進することが示唆され,バキュロウイルス感染における機能解明に役立つものと期待される。
バキュロウイルスは竿状でエンベロープ(外套)を纏い,2本鎖DNAで80 〜 180 kbp 長のゲノムをもったウイルスであり,主に蛾や蝶などの鱗翅目昆虫に感染する病原体である15。バキュロウイルスは,他のウイルスとは異なり,包埋型ウイルス(ODV)と出芽型ウイルス(BV)と称される2つの異なったビリオン表現型を形成する16。BVは昆虫体内での系統的な感染に必要であり,ODVは昆虫集団における水平的な感染を担う。ODVは高度に安定な結晶タンパク質マトリックスに被われ多角体と呼ばれる包埋体を形成する。初期感染は昆虫の中腸で開始され,昆虫の幼虫が餌(植物の葉)とともに多角体中のODVを摂取することから始まる。
バキュロウイルスは、特有の昆虫に感染し,ヒトを含む脊椎動物には感染しない。また,殺虫力が強く外部環境に安定な形態をしているため,森林や野菜などの病害虫を駆除する殺虫剤(農薬)としてよく使われている17。また,バキュロウイルスを用いたタンパク質発現系は哺乳類由来の遺伝子産物の大量生産に一般的で効率的な方法となっている18。タンパク質発現系に最もよく使われているバキュロウイルスはAcMNPVであり, sf9やsf21などの昆虫細胞株が宿主として用いられている。またBmNPVは,カイコの幼虫や蛹を宿主にして,組換えタンパク質の生産に利用されている19。
我々は,大腸菌K4株由来コンドロイチンポリメラーゼ(K4CP)20と各種ヒト由来硫酸基転移酵素の組換え体を用いて,明確な糖鎖長と硫酸基修飾含量をもつCS分子群を酵素化学的手法で合成し,CSライブラリーを構築した。そのCSライブラリーによって, CS糖鎖を認識する各種抗体やサイトカインを用いたCS分子種の生理機能の研究を行っている21。これらの実験の過程で,バキュロウイルス(AcMNPV)発現系によるコンドロイチン硫酸基転移酵素の調製を試み,その組換え酵素を用いて硫酸化反応を実施した。ところが,そのバキュロウイルス感染昆虫細胞の培養調製培地から得た組換え体画分がCS鎖を低分子化することに気が付いた。硫酸基転移酵素のcDNAを組み込んでいないバキュロウイルスを感染させた昆虫細胞の調製培養液にも明確なコンドロイチン分解活性が見られた。しかし,ウイルス感染していない宿主細胞培養液からはそのような分解活性はなかった。その活性画分はCS基質を232 nm の紫外線吸収を持つ二糖ないし四糖に分解した。 得られた二糖はHPLC解析により細菌由来コンドロイチンリアーゼが作る不飽和二糖標準品と同一であり,四糖はMSALDI-TOF質量分析により不飽和四糖に相当することが確認された。したがって,このバキュロウイルスが発現する酵素はコンドロイチンリアーゼであることが示唆された。そこで,そのウイルス感染細胞培養液中のリアーゼ活性を持つタンパク質を数段階のカラムクロマトグラフィーで精製した。その精製タンパク質は,ESI-MS/MS解析装置とタンパク質配列解析装置を用いることで,AcMNPV由来ODV-E66のN末端67アミノ酸残基から開始するN端欠損タンパク質AcODV-E66(67-704)であった13。
AcODV-E66は704個のアミノ酸からなり,分子量は全長で81 kDa と算出される,ODV包埋型ウイルスを被っているエンベロープタンパク質の一つである。我々は,N-末端アミノ酸の開始位置が異なる5種類の組換えタンパク質,すなわちAcODV-E66(67-704),AcODV-E66(70-704),AcODV-E66(100-704), AcODV-E66(24-704),ならびに全長タンパク質 [AcODV-E66(1-704)]にそれぞれN末端にHis6タグを付けた発現プラスミドを調製した。それら組換えタンパク質を大腸菌発現系で発現させ,DEAE-SepharoseおよびNi-Sepharose カラムクロマトグラフィーによって精製した。精製タンパク質のコンドロイチナーゼ活性を化学的に脱硫酸化したコンドロイチンを基質として用いて測定した(Table1)。
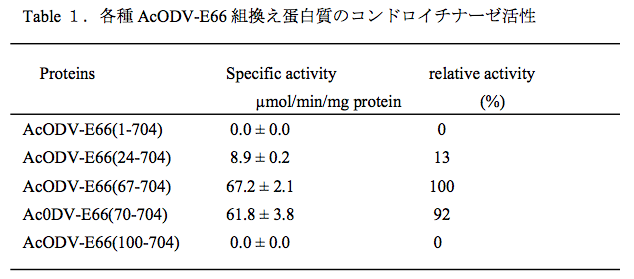
AcODV-E66(67-704) と AcODV-E66(70-704)は高いコンドロイチナーゼ活性を示したが,より長いAcODV-E66(24-704)は低い活性しか示さず,全長及びさらに短いAcODV-E66(100-704)は酵素活性を示さなかった。
バキュロウイルスAcMNPV由来コンドロイチナーゼ AcODV-E66 は広いpH範囲(pH 4〜9)と広い温度範囲(30〜60℃)を酵素活性領域に持つ安定な酵素であり,AcODV-E66の活性は二価金属イオンやキレート剤に影響を受けず,他の細菌由来コンドロイチナーゼとは異なった性質を持っていた。組換えタンパク質 AcODV-E66(67-704) の基質特異性を各種天然由来GAGを用いて調べた。調査した基質の中ではコンドロイチンが最も良い基質であり,異なった動物から調製したCSは全てコンドロイチンよりも低い分解性(16〜30%)であった。また,ヒアルロン酸には極めて活性が低く(0.16%)で,デルマタン硫酸やヘパリン,ヘパラン硫酸およびヘパロサンに対しては活性がなかった13。
基質特異性をさらに探求するために,我々は酵素化学的に調製した多糖体である合成コンドロイチン(sCH),合成コンドロイチン4硫酸(sCSA),および合成コンドロイチン6硫酸(sCSC)を用いた。それらは全て平均分子量1万であり,それぞれの二糖組成はsCHが0S 100%,sCSAは4S 92%、sCSCは6S 94% であった。その人工基質をAcODV-E66 (67-704) で処理し,その分解産物をゲルろ過クロマトグラフィーで二糖,四糖,及びそれ以上の糖鎖画分に分けて,それらの二糖組成を解析した(Fig. 2)。sCHとsCSC基質の大部分(99%)は二糖および四糖にまで分解され,それらの二糖組成は元の多糖体と類似していた。
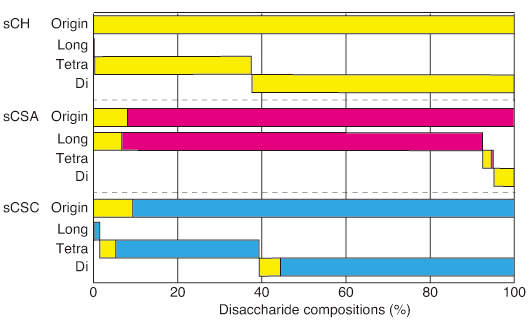
Fig. 2
AcODV-E66(67-704)で処理した合成多糖体(sCH, sCSA,およびsCSC)分解物から分離した二糖(Di),四糖(Tetra)そして長鎖糖(Long)画分の二糖組成,および分解前の合成多糖体の二糖組成.黄色,赤色,青色の棒はそれぞれ0S, 4S, 6Sの二糖単位を示す。
それに反し,sCSAは一部しか分解されず,反応後も四糖以上の長い糖鎖が93%も残った。少量のsCSA分解物である二糖および四糖の二糖組成は元の多糖体の組成と異なり大部分が0Sであった。しかし,切れ残った長い糖鎖画分の組成は元のsCSAの組成と同様に大部分が4Sであった。このようにODV-E66はCS構造に対して狭い基質特異性を示し,0Sと6S構造のみを切断し,他の二糖単位(4S,diSD,diSE, triSおよび他のGAG単位)は切断しなかった。
バキュロウイルス由来コンドロイチナーゼの切断位置を確定するために,複数のCS多糖体から本酵素で分解して得られた四糖画分を分離し,その非還元側二糖と還元側二糖の構造を解析した(Fig. 3)。クジラ軟骨由来のCSA,サメ軟骨由来のCSC,あるいはウシ気管由来のCSACをAcODV-E66(67-704)で処理し,反応混液からそれぞれの四糖画分 [CSA-4 (0S:4S:6S=7:46:47), CSC-4 (同5:24:71), and CSAC-4 (同7:42:51)] をゲルろ過クロマトグラフィーで分離した。その四糖の還元末端をアミノピリジン(PA)で標識し,コンドロイチナーゼACIIで二糖に分解した後,非還元側の遊離二糖をポストカラムHPLCシステムで解析し,還元側のPA標識二糖を蛍光HPLCシステムで測定した(Fig. 3A)。非還元側の二糖組成は0Sと6Sのみから構成されていたのに対し,還元側はODV-E66によって分解されない4Sも含まれていた(Fig. 3B)。これらの結果からODV-E66はエンド型のコンドロイチンリアーゼであり,0Sおよび6S二糖単位を認識し,その認識単位にあるGlcA残基の非還元側を切断する酵素であることが分かった。
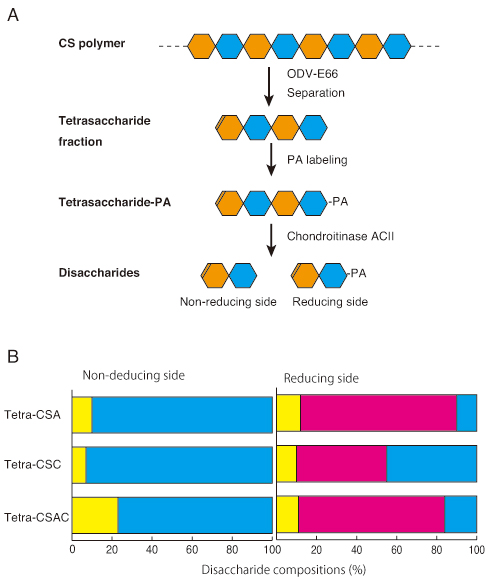
Fig. 3
A. 分解して得られた四糖の非還元端と還元端二糖の決定方法.天然CS多糖体をODV-E66で分解し,クロマトグラフィーで四糖画分を分離し,PAで還元端をラベルする。PA標識四糖をコンドロイチナーゼACIIで切断すると非還元端の遊離二糖と還元端のPA標識二糖が出来る。
B. 天然CSA, CSC, CSACのODV-E66分解物から分離したPA標識四糖画分の非還元側および還元側の二糖組成.黄色,赤色,青色の棒は0S, 4S, 6S二糖単位を表す。
つい最近,AcODV-E66の三次元構造がX線結晶構造解析法により決定された22。AcODV-E66の全構造は2つのドメインすなわちN端側のα-ヘリックスが豊富な領域とC端側のβ-ストランドが豊富な領域で構成されていた(Fig. 4A)。この立体構造はよく知られているコンドロイチナーゼACIやACIIおよびABC を含む多糖リアーゼ8(PL8)ファミリーにきわめて類似していた23。ところが,アミノ酸配列ではODV-E66とそれら細菌コンドロイチナーゼとは12%未満の相同性しかなかった。立体構造情報を元にアミノ酸配列を整列させると, ODV-E66はPL8ファミリー酵素の触媒領域の活性残基に相当する5つのアミノ酸残基(Asn236, His291, Tyr299, Arg345, および Glu395)をもっていた(Fig. 4B)。それら残基の置換変異体を調製し解析すると,それら全ては酵素活性に必須な残基であることを示した22。
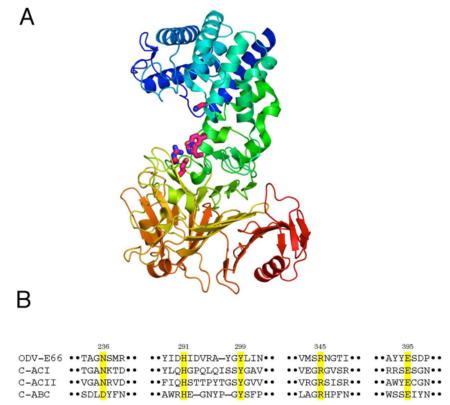
Fig. 4
A. AcODV-E66の結晶構造,触媒領域にある酵素活性に必須な5個のアミノ酸残基を示している。
B. AcODV-E66と細菌コンドロイチナーゼ(C-ACI, C-ACIIおよびC-ABC)の選択的に整列させたアミノ酸配列.触媒領域にある5個のアミノ酸残基を黄色の背景色で示す。
ODV-E66タンパク質をコードする遺伝子はほとんどのバキュロウイルス種の中で広く存在している。カイコ(Bombyx mori)に感染し死に至らせるバキュロウイルスBmNPVもODV-E66類似遺伝子を持っている。BmNPV由来のODV-E66(BmODV-E66)は全長で702個のアミノ酸残基を持ち,その配列相同性はAcODV-E66に対し92%もある。我々はBmNPVゲノムからBmODV-E66遺伝子をクローニングし,大腸菌発現用プラスミドを調製して,AcODV-E66(67-704)に相当する開始点を持つN-末端欠損タンパク質BmODV-E66(65-702)を発現させた(Fig. 5)。

Fig. 5 AcODV-E66 (Ac)とBmODV-E66 (Bm)の整列させたアミノ酸配列
星印は酵素活性に必須の5アミノ酸残基を示す。赤線は2つのN端切断組換えタンパク質のN-末端位置を示す。
その発現タンパク質BmODV-E66はAcODV-E66と同等のコンドロイチナーゼ活性を示し,活性pH範囲や温度範囲,基質特異性などの酵素特性はAcODV-E66と同じであった。両酵素ともCS鎖の0Sと6S単位をそのGlcA残基の非還元側で切断し,4Sおよび他の多硫酸化二糖単位を切断しなかった14。
バキュロウイルスが昆虫に感染するとき,ODV-E66がコンドロイチナーゼとして重要な役割を演じていると考えられる。バキュロウイルスにコンドロイチン分解活性が存在することは宿主昆虫がそのCS基質を持っていることを強く示唆している。宿主昆虫が外来物質の侵入を防ぐためにCSを持っており,バキュロウイルスが生産するコンドロイチナーゼが昆虫のCSを分解することで,ウイルス感染を促進しているかもしれない。
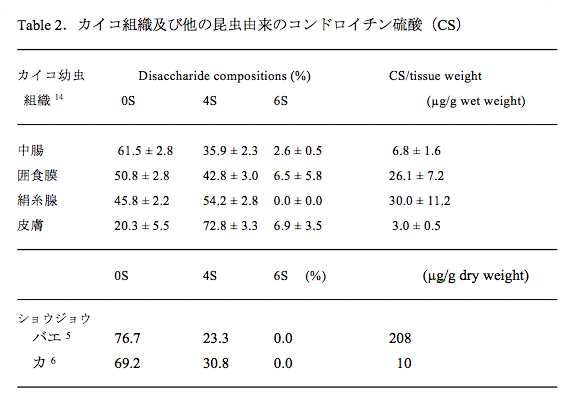
したがって我々は,扱いや入手のしやすさと上記BmNPVが感染することから,カイコ幼虫(Fig. 6)を宿主昆虫の代表として研究を行った14。カイコ五齢幼虫の複数の組織からGAG画分を抽出・精製し,そこに存在するCSの量と二糖組成を解析した(Table 2)。CSは中腸,囲食膜(PM),絹糸腺,および皮膚などの昆虫組織に存在していた。囲食膜とは昆虫の中腸腔側に位置し,中腸上皮組織と摂食した食餌とを分離する無細胞の膜状組織のことである24。組織重量あたりのCS量は絹糸腺で最も多く,次いで囲食膜,そして中腸と皮膚の順であった。CSの硫酸化度は中腸,囲食膜と絹糸腺で38〜54%あり,皮膚では80%と高かった。カイコCSの硫酸化二糖単位は主に4Sであるが,中腸や囲食膜および皮膚で6Sも確かに存在していた。ただし,2硫酸化や3硫酸化二糖は検出されなかった。

Fig. 6 カイコ幼虫(五齢虫)の写真
ショウジョウバエ5や蚊6のような他の昆虫では,0Sが中心でそれに4Sが少しある程度の低硫酸化CSが存在すると以前に報告されている(Table 2下)。ショウジョウバエのL3期の胚のCSには6S単位が確かに存在するとの報告が一報あるが25、本研究では硫酸基位置特異的なコンドロイチンスルファターゼを用いて,カイコ組織中のCSに6S単位が確かに存在することを示した。興味深いことに,CSの二糖組成はカイコの組織毎に異なっている。このことは生体内でCSを合成する各組織において,コンドロイチン4−硫酸基転移酵素と6−硫酸基転移酵素の発現レベルが異なっていることを示唆している。また, 6S単位を含み多くが0Sである中腸や囲食膜のCSは,0Sと6S構造を好むODV-E66コンドロイチナーゼの基質特異性との関連性が高いと考えられる。
次に,免疫組織学的によりカイコ幼虫のCSの分布を探求した14。カイコ五齢幼虫の全身縦断切片を,抗CS抗体であり無硫酸コンドロイチンを優先的に認識する,473抗体26で染色した(Fig. 7)。473抗体はカイコ幼虫の中腸,絹糸腺,および皮膚組織を含む多くの組織を染めた。中腸においては,抗体は囲食膜,円筒上皮細胞の微絨毛や基底膜を強く染めた(Fig. 8A)。H-E染色では上皮細胞は強く染まるが,囲食膜の染色は弱かった(Fig. 8B)。囲食膜は中腸上皮と摂食餌との間で複数の0.2〜1 µmの薄い層からなる細胞外マトリックスとして観察される。絹糸腺では,細胞層の外側および内側基底膜が抗体により免疫染色された(Fig. 8C)。皮膚組織では,表皮外面の外表皮と,表皮・真皮の間隙や,真皮内側基底膜,および脂肪体の表層基底膜などが抗CS抗体で染まった(Fig. 8E)。他の各種抗CS抗体を用いた免疫組織化学解析では,異なったCS構造を認識して特有な組織分布を示した14。
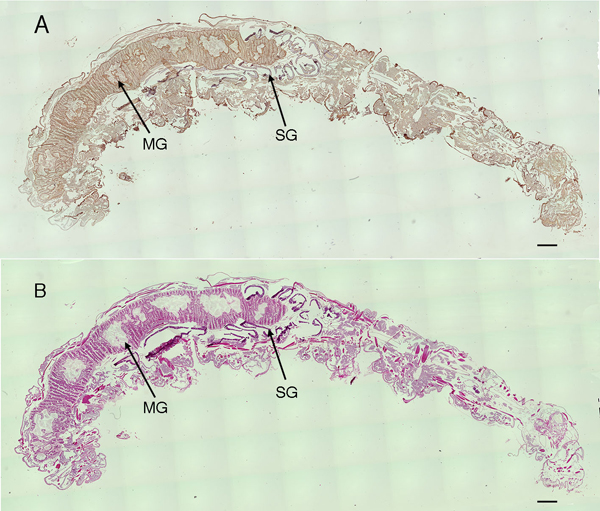
Fig. 7 カイコ幼虫全身の縦断切片
473 抗体による染色(A)とH-E染色(B).MGは中腸,SGは絹糸腺を示す。スケールバーは500 µmを示す。
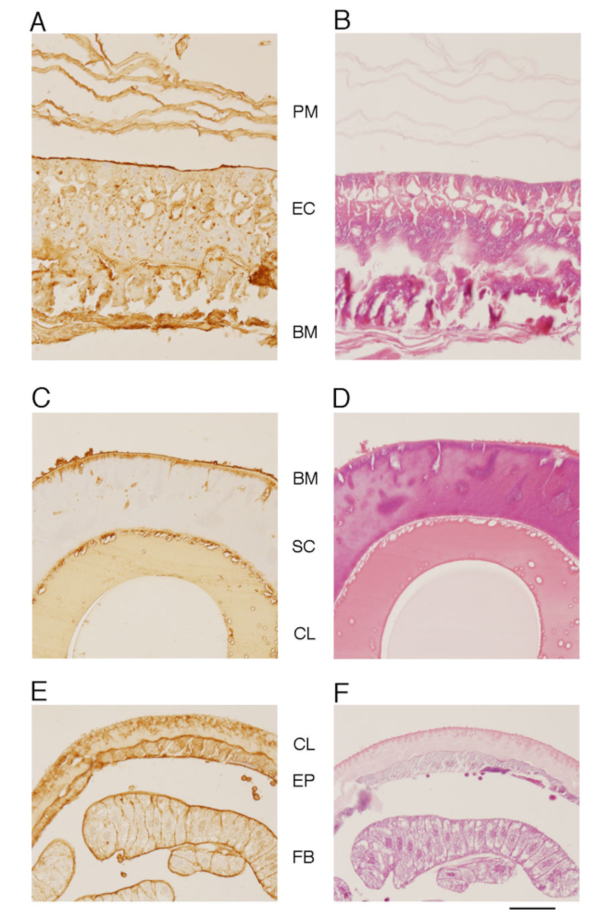
Fig. 8 カイコ幼虫の中腸(A, B)絹糸腺(C, D)および皮膚(E, F)の組織化学的解析
カイコ組織の横断切片を473 抗体(A, C, E)とH-E(B, D, F)により染色した。PMは囲食膜,ECは上皮細胞,BMは基底膜,SCは絹糸腺細胞層,CLは絹質層あるいは表皮,EPは真皮,FBは脂肪体を示す。スケールバーは20 µmを示す。
ODVを形成するバキュロウイルス多角体は植物と共に昆虫の幼虫に摂食され,中腸に移動し,高いpHと分解酵素によって可溶化される。遊離されたウイルス竿は,中腸上皮と食餌とを隔てている囲食膜を通過して,中腸上皮細胞に感染する(初期感染)。上皮細胞中でBVが作られ,昆虫体内全体に感染が広がる(第二感染)。その後,ODVが昆虫細胞の核中で作られ,昆虫体の崩壊によって多角体として外部環境に放出される(後期感染)。けれども,このバキュロウイルス感染機構の詳細は未だ不明確である。
囲食膜は,前中腸から後腸にかけて,複数層の筒状形態で中腸内腔に広がる細胞外マトリックスであり,キチンや糖タンパク質およびCSプロテオグリカンで構成され,親水性と弾力性に富んだ組織である。囲食膜は中腸上皮を摂食物質の機械的障害や毒性から保護し,病原体の感染に対するバリヤーとしての役割を果たしている。
最近,Xiangら27は,ODV-E66欠損AcMNPVウイルス株は宿主昆虫への経口投与において,50%致死させるのにコントロールウイルスに比べて,千倍高いウイルス量が必要であると報告した。しかし,そのODV-E66欠損変異株BVの培養昆虫細胞Sf9への感染はコントロールウイルスと変わらなかった。このことはODV-E66エンベロープタンパク質はバキュロウイルスの経口感染に重要な役割を演ずるが,ウイルス複製の段階では必須ではないことを示している。また,AcODV-E66の類似配列を持つペプチドが鱗翅目昆虫の中腸上皮に結合し,バキュロウイルス感染を拮抗阻害することが別の文献で書かれている28。我々はまた,囲食膜由来のCSがBmODV-E66コンドロイチナーゼによって実際に分解されることを示した。
いくつかの実験事実から以下のことが示唆される。 初期感染の際には,宿主昆虫の中腸内アルカリ環境下において,ウイルス包埋体の溶解に伴ってODV-E66エンベロープタンパク質は遊離し,中腸内プロテアーゼによりN末端ペプチドが切断されて活性化する。その活性化したウイルス由来コンドロイチナーゼは囲食膜中のCSを分解し,その破壊された囲食膜を通過してODVの上皮細胞への侵入を促進すると考えられる(Fig. 9)。
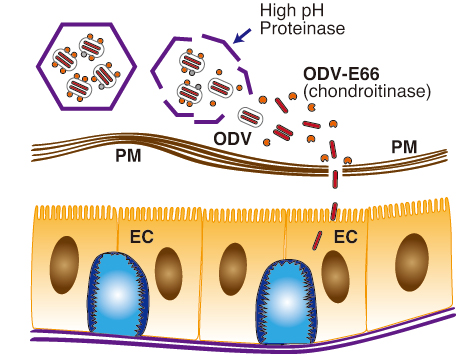
Fig. 9 バキュロウイルスの初期感染における仮説図
昆虫の幼虫に経口摂食されたバキュロウイルス多角体は高pHと分解酵素によって昆虫の中腸内で可溶化する。同時に,ODV-E66エンベロープタンパク質も遊離し,切断・活性化されコンドロイチナーゼ活性を獲得する。そして,囲食膜中のCSを分解することによりバキュロウイルスの中腸上皮細胞への感染を促進すると考えられる。
本稿ではバキュロウイルス由来の新規なコンドロイチナーゼの発見と,カイコ組織におけるCSの分布,およびウイルスコンドロイチナーゼによる宿主昆虫へのバキュロウイルス感染機構の仮説について記述した。今後もin vivo でのバキュロウイルスの昆虫への感染におけるメカニズムの解明への手がかりを提供していくつもりであり,さらに脊椎動物と同様に昆虫におけるCSの生理学的機能を解明していきたい。
謝辞
結晶構造の図を提供していただいた九州大学の角田佳充博士に感謝申し上げます。また,本研究は日本文部科学省の科学技術研究費(# 23570176)と私立大学戦略的研究基盤形成支援事業助成金(S1101027)の支援を受けて行った。