
氏名:鈴木 匡
1992年東京大学理学部生物化学科卒業。1997年東京大学大学院理学系研究科生物化学専攻博士課程修了(指導教官:井上康男教授および榎森康文助教授)。1997年より2000年まで、ニューヨーク州立大学ストーニーブルック校生化学/細胞生物学教室ポストドクトラルフェロー。2000年より同大学にて研究助教授。この間、出芽酵母の細胞質ペプチド:N-グリカナーゼ(PNGase)遺伝子およびヒト細胞質エンド-β-N-アセチルグルコサミニダーゼ(ENGase)遺伝子の同定を行った。2001年12月より日本科学技術振興事業団(JST)さきがけ研究21(PRESTO)研究者。翌年2月より生物情報科学学部教育特別プログラム(UPBSB)科学技術振興特任教員(東京大学大学院理学系研究科生物化学専攻)。PNGaseおよびENGaseといった脱糖鎖酵素の構造と機能について研究をすすめている。
ペプチド:N-グリカナーゼ (PNGase; 別名グリコアミダーゼ/N-グリカナーゼ) は糖タンパク質/糖ペプチドのアスパラギン型(N型)糖鎖を脱離する糖鎖脱離酵素である。植物およびバクテリアより単離された本酵素はこれまでN型糖鎖の構造および機能の研究の際の有用な試薬として広く用いられてきたが、不思議なことに酵素自体の生理機能に関してはこれまで殆どといってよい程研究の対象にされてこなかった。
真核細胞の細胞質中に広く存在するPNGaseは、これまで新生糖タンパク質の品質管理機構、とりわけ変性糖タンパク質のプロテアソームによる分解系に関与することが様々な研究より示唆されてきている。ここでは本酵素の構造および機能についての最新の知見を概説したい。より詳しい総説については文献1, 2を参照されたい。
真核細胞において、分泌経路を通るタンパク質は細胞質で合成され、そのうち可溶性なものは小胞体(ER) 膜を通過してルーメン内に取り込まれ、一方膜貫通タンパク質はここで膜に埋め込まれる。即ちERはそのようなタンパク質が様々な場所へ運ばれる際の配送拠点のような役割を果たす。一方、このオルガネラはタンパク質の配送の前に、その正しい折り畳み構造やサブユニット形成(高次構造)を厳しくチェックする機能も兼ね備えており、遺伝子の変異や代謝過程によって生じた“出来損ない”あるいは“不必要”なタンパク質を正しい構造に直したり、取り除いたりしている。このような校正、除去機構は“品質管理”機構と呼ばれ、細胞内に不要なタンパク質が蓄積するのを防いでいる。具体的には、異常な高次構造をとるタンパク質はルーメン内で様々な分子シャペロンによって捕らえられ、正しく機能的な構造をとれるような手助けをうける。しかしながらシャペロンの助けをうけてなお修復が難しいようなタンパク質はやがて“小胞体関連分解(ERAD; ER-associated degradation)”という機構によって分解をうける3。この機構は3段階からなる。即ち、(I)異常タンパク質のER内での感知、(II)それらのERAD基質のER膜上、およびルーメン内から細胞質への逆輸送(retrotranslocation)、そして(III)ユビキチン-プロテアソーム系によるタンパク質分解、という過程である4。最近ではERADの内、特にN型糖鎖を持つタンパク質用に働く分解機構が明らかになってきており、GERAD(glycoprotein ERAD;糖タンパク質のERAD)という言葉も使われはじめている 5。このERAD/GERAD機構の詳細を解明することは基礎生物学的な興味の他に、ヒト疾患の新たな治療法の開発といった医学的見地からも非常に重要である。実際、この監視システムの不備、異常によってタンパク質の機能が損なわれる、あるいは毒性を発現することによって起こる先天的あるいは後天的疾患は数多く存在するのである。
細胞質PNGaseは最初にWiertzらによってERAD機構に関与する酵素であることが実験的に示唆され6、以来酵母からヒトに至る迄幅広い系においてその仮説が支持されてきた1. PNGaseによる糖鎖の脱離は、立体的に嵩高い糖鎖を糖タンパク質のアミノ酸側鎖から外すことによって、それらがシリンダー状の構造の内部に存在するプロテアソームの活性中心により効率良く届くようにしていると考えられている。しかしながら少なくとも出芽酵母においては、本酵素を欠損しても高次構造不全の糖タンパク質は(分解速度は遅まるものの)問題なく26Sプロテアソームによって分解を受ける7。よって、糖タンパク質もPNGaseの助けを借りずに分解されることは可能のようである。一方、現在の20Sプロテアソームの立体構造のモデルでは、N型糖鎖のついたタンパク質がそのままの形でプロテアソームのシリンダー内の活性中心に到達し、また分解後に出て行くといったシナリオは考え難い8。しかもユビキチンリガーゼのようにPNGaseが重複性を持つとは遺伝子および生化学的解析からは考えられず7,8、どのようにプロテアソームがPNGase非存在下で糖タンパク質を分解しているのかは、興味深い問題である。
最近我々はPNGaseの遺伝子(PNG1)を出芽酵母より初めて同定す7ることに成功した。その配列をもとに、各種データベースを用いてオルソログの検索を行ったところ、本酵素は真核細胞おいて非常に良く保存されていることが明らかになった。出芽酵母や分裂酵母では、良く保存された“コア”ドメインのみを持つ、いわば“プロトタイプ”の酵素ともいえる構造であるのに対し、多細胞生物由来の酵素はN端とC端の両側に延長したドメインを持つ。 これらのPNGaseの一次構造上の特徴は、そのもっとも保存された部位に“トランスグルタミナーゼ”モチーフを持つことである。それゆえ、本酵素は“トランスグルタミナーゼスーパーファミリー”の一員として分類されている9。トランスグルタミナーゼはグルタミンとリジンの側鎖に共有結合を作ることによってタンパク質間の架橋を作る酵素である(図1)。トランスグルタミナーゼスーパーファミリーに属するタンパク質は、一般にチオールプロテアーゼに類似したCys, His, Aspのトライアドによる活性中心を持つ。これらの分子には酵素としてはこれまでトランスグルタミナーゼ(アミド結合の生成)とプロテアーゼ(アミド結合の切断)が知られている。一方PNGaseはグリコシルアミン結合を切断するアミダーゼであり(図1)、これら3つの酵素がいずれもアミド結合の生成、および切断を触媒していることから、PNGaseがトランスグルタミナーゼ・スーパーファミリーの第3のメンバーを構成することもそれ程驚きではない。実際それらのトライアドは調べられた範囲で全てのPNGaseオルソログに保存されている。更に、本酵素活性がin vitroでフリーの-SH基を必須とすることも10, 11、Cys残基が求核基として活性中心の一部を成すという仮定と符合する。ごく最近、出芽酵母PNGaseの種々の点変異体の網羅的解析によって、実際それらの残基が酵素活性中心を構成し、本酵素がトランスグルタミナーゼと共通の祖先を持つ親戚ともいえる酵素であることが強く示唆された12。
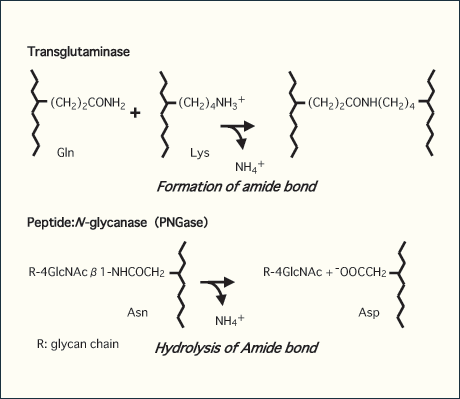
図 1 トランスグルタミナーゼ (上) とペプチド:N-グリカナーゼ(下)の反応
トランスグルタミナーゼはGluとLys残基の側鎖間のアミド結合の生成反応を担うのに対し、PNGaseは グリコシルアミン結合の加水分解を行い、 還元末端にジ-N-アセチルキトビオース構造を保持した遊離糖鎖と糖が結合したアスパラギン残基がアスパラギン酸残基に変換した脱糖鎖タンパク質あるいはペプチドを生じる。
最近我々は、本酵素がRad23タンパク質(Rad23p)と生体内で複合体を形成することを明らかにした13, 14。RAD23はもともとDNA修復に関わる遺伝子として取られたものであるが、その産物は現在では非常に多岐の現象に関わる多機能性を有することが分かっている。Rad23pは、そのN端に存在するユビキチン様ドメインを介して26Sプロテアソームと結合し得ることも明らかにされている。実際出芽酵母においては、PNGase(Png1p)はRad23pを介して26Sプロテアソームと結合することが明らかとなった。Rad23p-Png1pの複合体は、これまで見い出されていたDNA修復に必要なRad23p-Rad4p 複合体とは別々に存在している。また、Rad23pに2ケ所存在するUBA(Ubiquitin-Associated)ドメインは、26Sプロテアソームによる分解の主要なシグナルであるユビキチン/マルチユビキチン鎖と結合することが明らかとなっている。これらの結果から、Rad23pが26SプロテアソームとPNGaseを始めとした様々な分子を物理的に繋ぎ合わせ、結合タンパク質の安定性や機能の制御をおこなう“エスコート”タンパク質としてその多機能性を発揮することが示唆された。
更に最近、哺乳動物あるいはショウジョウバエ由来のPng1pの延長したN端部分に、PUB/PUGドメインと名付けられた新規な配列モチーフが見い出されたのは特に興味深い 15, 16。このドメインを持つオルソログにおいて種間のドメイン配列は非常によく保存されている一方、真菌類や植物由来のオルソログにはこのドメイン自体存在しない。我々の予備的実験から、PUB/PUGドメインはユビキチン/プロテアソームと関連する分子群と結合するのに重要な役割を果たしていることが示唆されている14。興味深いことに、見い出された分子のうち(酵母Png1pと共通に存在する)コアのドメインを結合に必要とするのはRad23pオルソログのみで、他の全ての分子はPUB/PUGドメインを含むN端ドメインに特異的に結合することが分かった。
PUB/PUGドメインの機能的役割についてはまだ不明な点が多い。しかしながら特筆すべき点は、PUB/PUGドメインを持つタンパク質の中にはしばしばUBA、あるいはUBXドメインといった、ユビキチン関連の経路に関わる酵素群などによく見られるドメインを同時に合わせもつ機能未知タンパク質が見出されることである。UBAおよびUBXドメインは、もともとユビキチンに関連した酵素/タンパク質に多く見出されていた配列モチーフある。最近UBAと、そして恐らくUBXドメインもタンパク質間相互作用ドメインとして機能していることが分かってきている17。我々の実験結果を考えあわせると、PUB/PUGドメインもUBAや恐らくUBXと同様、タンパク質間相互作用を担うドメインの一員である可能性がある。もしその仮説が正しいとすると、これらのドメインはUBAやUBXと協同して複雑なタンパク質間相互作用のネットワークを形成するのに役立っていると考える事ができる。そしてこれらのネットワークは例えばユビキチン-プロテアソーム系のような素過程において重要な働きを果たしているのかもしれない。こう考えてみると、哺乳動物あるいは昆虫のオルソログにおいて細胞質PNGaseがPUB/PUGドメインを獲得したことは、タンパク質相互作用を生み出す上で大きな利点をもたらした進化の結果と考えることが出来る。細胞質における高次構造不全のタンパク質の分解は、実際はさまざまなタンパク質修飾の連鎖的反応を伴う。即ち、PNGaseによるユビキチン化、糖鎖の脱離、脱ユビキチン化といった反応である。PUB/PUGドメインの獲得は、これらの一連の操作を効率よく一所で行う“糖タンパク質分解複合体”とも呼べるようなプラットホームを形成するのを可能にしたのかも知れない2。今後はこのような複合体の存在を明らかにすると共に、構成分子を同定していくことで、仮説の検証が行われることが期待される。
細胞質PNGaseが実際にGERADに関与する分子だということは、幾つかの実験から示された。まずER内のN型糖鎖をもつ小ペプチドは高次構造不全の糖タンパク質と同様に細胞質に逆輸送されることが知られているが、これらは細胞質のPNGase活性によって糖鎖の脱離をうける18, 19。また、プロテアソームの阻害剤を加えることで、細胞質に蓄積する(主に出芽酵母ではPNGaseの反応によって生じることが最近示されたが20)遊離のN型糖鎖の量が顕著に減少することも示され、プロテアソームによるタンパク質分解とPNGaseによる糖鎖の脱離が共役した反応であることが示唆された21。更にごく最近、PNGaseがGERADの基質となる糖タンパク質にも働きうることが示され、本酵素による糖鎖の脱離は実際26Sプロテアソームによる分解の前に起こる、という仮説が支持された8。興味深いことに、細胞質PNGaseはタンパク質のフォールディングを見分ける能力があり、変性した糖タンパク質の糖鎖のみを外すようである8。ごく最近ディスロコンがトランスコロンと異なり、高次構造を保ったタンパク質をも膜を通過させ得ることが報告されている22ことから、少なくともあるケースにおいてはPNGaseが働く為に何らかのタンパク質の“巻き戻し(unfolding)”のステップが必要であることは想像に難く無い。
ごく最近、レクチン-ユビキチンリガーゼFbx2がGERADの過程で重要な役割を果たしていることが示された23。このレクチンはSCF(Skp1-Cullin1-F box)複合体を形成し、ユビキチンをタンパク質に修飾するE3ユビキチンリガーゼとして働く。このSCFFbx2複合体はN型糖鎖を介して糖鎖を持つERAD基質を認識し、基質のユビキチン化を行うことが明らかとなった23。その反応機構を考えると、この SCFFbx2複合体による基質の認識はPNGaseによる糖鎖脱離の前に起こると考えられる(図2)。
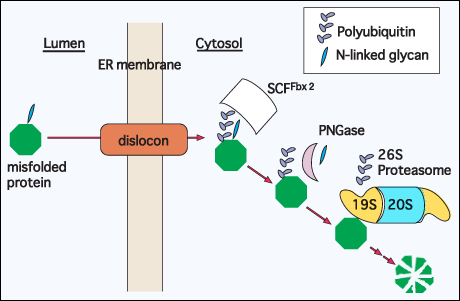
図 2 高次構造不全の糖タンパク質の分解の仮想モデル:細胞質における出来事
ある糖タンパク質がERにおいて正しい高次構造をとれなかった場合、それらのはdisloconというタンパク質チャネルを通してERから細胞質に放出される。細胞質ではまず糖タンパク質特異的リガーゼである SCFFbx2複合体によって認識され、ポリユビキチン化される 23。次いでN型糖鎖はPNGaseによって外され、さらにポリユビキチン鎖はプロテアソームの19SサブユニットであるRpn11pによって除かれ25, 26、最終的にプロテアソームによる分解をうける。
1993年当時、我々が初めて哺乳動物培養細胞の細胞質画分に本酵素活性が見出した時は、“なぜ細胞質に??”という根本的な疑問に悩まされたものであった。その当時(当然酵素の基質であると考えられる)N型糖鎖を持つ糖タンパク質が細胞質に存在する、ということを信じる研究者は殆どいなかったのである。しかしながらそれから10年の月日が流れ、今では糖タンパク質の細胞質への“逆輸送”は当たり前のように語られ、細胞質PNGaseの存在はおろか、GERAD過程に関わる重要な一構成分子であることに疑問を投げかけるものは殆どいない。今後は高等動物の細胞および個体におけるPNGaseの生理機能の解明、とくにその欠損が及ぼす表現型の詳細な解析が興味ある課題といえよう。