Jan. 22, 2003
成長因子ミッドカインのシグナリングにおけるコンドロイチン硫酸Eの役割(2003 Vol.07, A1)
村松 喬
氏名:村松 喬
村松博士は東京大学を1963年に卒業し、その後Albert Einstein医科大学の微生物学免疫学講座のポスドクトラルフェロー、神戸大学医学部生化学第一講座の助教授、Pasteur研究所分子生物学講座の客員研究員(visiting scientist)を経て、鹿児島大学医学部生化学第二講座の教授となった。現在名古屋大学大学院医学系研究科生物化学講座(旧生化学第一講座)の教授である。また、日本生化学会の会長そして、Glycobiology誌執行編集長として活躍している。
1. はじめに
コンドロイチン硫酸は通常2糖あたり1つの硫酸基を含んでいる。しかしながら2つの硫酸基を含む過硫酸コンドロイチン硫酸が存在する(図1)。最初に見つかったのはサメ軟骨中のコンドロイチン硫酸Dであった1,2。その基本的構造はコンドロイチン-6硫酸で、ウロン酸残基の多くに2-硫酸がある。その後コンドロイチン硫酸Eがイカ軟骨で見つかった2,3。その基本的構造はコンドロイチン-4硫酸で、N-アセチルガラクトサミン残基にしばしば6-硫酸がついている。その後の研究からほ乳動物の細胞中にも、過硫酸構造の存在が明らかになった4,5。ここではコンドロイチン硫酸D中で見つかった過硫酸の構造をDユニットと呼び、コンドロイチン硫酸E中にある構造をEユニットと呼ぶ。過硫酸構造の生物学的意義については、長い間ほとんど分からなかった。しかしながら最近の研究で過硫酸構造はミッドカイン6-8、ケモカイン9、L-セレクチン9と結合することで細胞表面の識別に関与していること、神経突起伸長の制御に関係していることが明らかになった10。この概説ではコンドロイチン硫酸E構造とミッドカインの強い相互作用とその意義について論じる。まずは、ミッドカインについて手短に述べる。

図 1 コンドロイチン硫酸の構造
2. ミッドカイン
ミッドカインは分子量13-kDaのタンパク質で、多くの細胞の成長、遊走、生存を増強させる。ミッドカインはプレイオトロフィン/HB-GAMと50%の配列同一性があるが、他の成長因子やケモカインとは類似しない11,12。
ミッドカインは基本的にジスルフィド結合で固く結ばれた2つのドメインからなり、それぞれには3つのアンチパラレルなβシートがある13。塩基性アミノ酸の2つのクラスターが、よりC-末端側に位置したドメイン中にあり、グリコサミノグリカンの結合部位として働く13。
ミッドカインは発生中期に強く発現するが、成体組織では特定の部位でのみ検出される12,14。しかしながらミッドカインは多くのヒト固形がん、さらに、炎症・修復部位で強く発現されるようになる。12,15-17。ミッドカインのアンチセンスオリゴDNAはヌードマウスでの大腸がん細胞の増殖を抑制する18。従ってミッドカインはがん細胞の悪性化に、おそらく成長、生存、浸潤を増強することで、寄与するらしい。ミッドカインはまた炎症細胞の遊走を促進させる。ミッドカイン遺伝子欠損マウスでは、血管傷害による動脈の内膜新生16や虚血傷害後の腎炎17が有意に抑制される。これらの現象の理由としては、欠損マウスでは炎症細胞の遊走が減少していることが考えられる。一方、ミッドカインの生存促進活性は、神経変性の抑制を期待させる。定常光を連続的に照射して発症させた網膜変性はミッドカインで抑制される19。虚血傷害後に起きる海馬の遅発性神経細胞死もミッドカインで抑制された20。さらにin vitro で発育させた移植前段階の胚の生存率はミッドカインで増加する21。従ってミッドカインは分子標的療法のターゲットとして、また変性疾患の治療に使えそうな薬剤として重要な因子である。
ミッドカイン受容体は膜貫通タンパク質と膜貫通プロテオグリカンの両者で構成される分子複合体である。膜貫通タンパク質としては、低密度リポタンパク質受容体関連タンパク質 (low density lipoprotein receptor-related protein (LRP))が重要な役割を演じる22。さらにALKチロシンキナーゼがミッドカインシグナリングに関与することが、最近報告された23。プロテオグリカンでは、シンデカンとコンドロイチン硫酸プロテオグリカンが、共にミッドカインのシグナリングに関係する6,12。ミッドカインの細胞内シグナリングシステムにはPI3キナーゼとERKが含まれる12,24。
3. ミッドカインによるコンドロイチン硫酸Eの識別
コンドロイチン硫酸Eとミッドカインの相互作用は2つのアプローチで明らかにされた。まず、ミッドカインはコンドロイチン硫酸プロテオグリカンである受容体型タンパク質チロシンホスファターゼζ(ゼータ)(PTP ζ )と強く結合することが分かった6 (図2)。胚の神経細胞のミッドカイン依存性の遊走では、PTP ζがミッドカインの受容体であることが、以下のことから証明された。1) コンドロイチナーゼABCで神経細胞を処理するとミッドカインの作用が消失する。2) PTP ζの細胞外部分に対する抗体はミッドカインの作用を阻害する。3) ミッドカイン変異体へのPTP ζの結合能とその遊走促進活性とは良く相関する。PTP ζはまた、ミッドカイン依存性の骨芽細胞様細胞の遊走25およびミッドカイン依存性の胚の神経細胞の生存26に関与している。
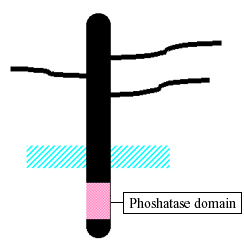
図 2 受容体型タンパク質 チロシンホスファターゼ ζ (PTP ζ )
ミッドカインはPTP ζのコンドロイチン硫酸部分と高親和性で、タンパク質部分と低親和性で結合する6。ミッドカインがどの様なコンドロイチン硫酸と強く結合するか調べるために、種々のコンドロイチン硫酸を用い、ミッドカイン依存性の遊走に対する阻害効果を調べた。コンドロイチン硫酸の中で、コンドロイチン硫酸Eが最も強く細胞遊走を阻害することが分かった。
我々はまた、ミッドカインは細胞周囲のコンドロイチン硫酸プロテオグリカンであるPG-M/バーシカンに高親和性で結合することを明らかにした27。この結合はヘパリン、コンドロイチン硫酸DおよびEで阻害されたが、PG-Mのコンドロイチン硫酸中には少量のDユニットとEユニットが検出された。
コンドロイチン硫酸Eはミッドカインをコートした培養皿の神経突起伸長を阻害したが7、このことでもう一つの方向の研究が始まった。他のコンドロイチン硫酸はこの系に対して阻害効果を示さなかった28。ヘパリンがミッドカインに対して強く結合することは既知であるので、コンドロイチン硫酸Eとヘパリンのミッドカインに対する結合親和性を比較した。解析法として表面プラズモン共鳴(SPR)7とミッドカインセファロース−アフィニティークロマトグラフィー8、そして神経突起伸長抑制作用を用いた7,28。その結果、コンドロイチン硫酸Eはヘパリンと同程度に強くミッドカインに結合することが判明した。
ミッドカインに応答する細胞にはEユニットを豊富に含むコンドロイチン硫酸があるのか検討する必要があった。そこで、13日齢マウス胚の脳を用いて合成されたコンドロイチン硫酸を分析したところ、コンドロイチン硫酸画分には強くミッドカインに結合する画分があり、これは多量のEユニットを含んでいた8。
つぎに、コンドロイチン硫酸Eの修飾、例えばグルクロン酸の3-O-硫酸化29の様なものがミッドカインへの結合に関与するのか調べた。我々は、精製した、あるいはリコンビナントのコンドロイチン4-硫酸6-硫酸転移酵素を用いて、コンドロイチン4-硫酸から人工的にコンドロイチン硫酸Eを合成し、実験に用いた30。合成コンドロイチン硫酸Eはミッドカインに強く結合し、3-O-硫酸化のような修飾は強い結合に必要ではないことが示された8。また強い結合にはEユニットのクラスター化が必要であることも分かった。
ミッドカインのヘパリンあるいはヘパラン硫酸との強い結合には、ヘパリントリ硫酸ユニット中の3つの硫酸基全てが必要である31。ミッドカインとの強い結合に必要な2糖単位あたりの硫酸残基数が、コンドロイチン硫酸Eではヘパリンに比べ少ないことが注目される(図3)。
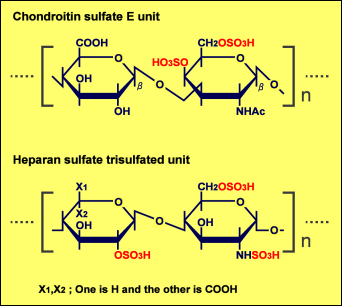
図 3 ミッドカインと強い結合能を持つ2つの構造の比較
Eユニットのクラスターはコンドロイチン硫酸鎖中に広く分布しているわけではない。従ってこの構造は、ミッドカインとの結合、さらに他の分子との結合において特別なシグナルとして働くことができよう。
4. コメント
我々の研究により、コンドロイチン硫酸Eユニットがミッドカインと強く結合すること、そしてミッドカインのシグナリングに関与することが確かなものとなった。しかしながらミッドカインのシグナリングにおけるこの結合の正確な役割は、今後のさらなる研究で明らかにされる必要がある。おそらくミッドカインはコンドロイチン硫酸プロテオグリカンPTPζと結合してこれを2量体化し、そのことでホスファターゼ活性が不活化されるであろう。ただし、ミッドカイン受容体は分子複合体であることから、コンドロイチン硫酸部分への結合がコンドロイチン硫酸プロテオグリカンと複合体の他の構成成分との関係を変化させる可能性も残っている。
ケモカイン9とセレクチン9もまた、コンドロイチン硫酸Eに結合するという知見は、かなり多くの識別分子が過硫酸コンドロイチン硫酸に結合することを示唆している。ヘパリン結合性識別分子には、ヘパリン/ヘパラン硫酸を特異的に識別するものと、ヘパリン/ヘパラン硫酸と過硫酸コンドロイチン硫酸を共に識別する二重識別能を持つものがあるのであり、この分類が緊急課題である。最近、FGF-16、FGF-18とHB-EGFもコンドロイチン硫酸Eに強く結合することが報告された32。
過硫酸コンドロイチン硫酸の生体内での識別の意義を確立することは同様に重要なことである。コンドロイチン硫酸DとEは図4に概略示した様な経路で合成される。コンドロイチン硫酸6-硫酸転移酵素のノックアウトマウスでは、脳内にコンドロイチン硫酸Dが検出されなかった33。今までのところ、欠損マウスの脳に異常は見つかっていない。おそらくノックアウトマウスの脳内にはコンドロイチン硫酸E構造が残っているので、D構造の消失を補ったと考えられる。
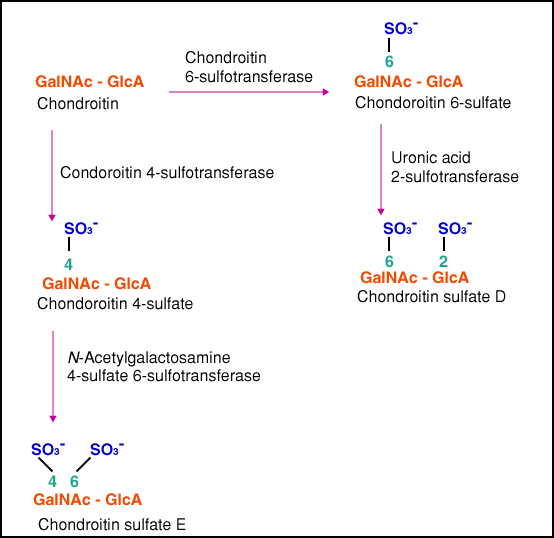
図 4 過硫酸コンドロイチン硫酸の生合成経路
Keyword
コンドロイチン硫酸:コンドロイチン硫酸の基本構造はコンドロイチンで、その繰り返しユニットはN-アセチルガラクトサミンとグルクロン酸からなる2糖である。異なる水酸基が硫酸化されることで、異なるコンドロイチン硫酸が生じる。コンドロイチン4-硫酸の、グルクロン酸のC-5位の水酸基がエピマー化することでデルマタン硫酸が生じる。コンドロイチン硫酸構造中に微細な多様性があることは、大きな特徴である。例えば、材料の違いでコンドロイチン硫酸の過硫酸化の程度は異なる。コンドロイチン硫酸の構造解析には鈴木旺教授の開発したコンドロイチナーゼが不可欠である。コンドロイチナーゼABC消化によって、コンドロイチン硫酸は不飽和2糖に分解されるので、これらをHPLCで分別し定量する。
References
- Suzuki S: Over-sulfation of mucopolysaccharides - A historical review in Different Slices of Biochemistry (S. Suzuki et al, Eds), Kodansha, pp24-38, 1971(Japanese)
- Suzuki S, Saito H, Yamagata T, Anno K, Seno N, Kawai Y, Furuhashi T: Formation of three types of disulfated disaccharides from chondroitin sulfates by chondroitinase digestion. J.Biol. Chem., 243, 1543-1550, 1968
- Kawai Y, Seno N, Anno K: Chondoroitin polysulfate of squid cartilage, J. Biochem.(Tokyo), 60, 317-321, 1966
- Saigo K, Egami F: Purification and some properties of acid mucopolysaccaride of bovine brain. J. Neurochem., 17, 633-647, 1970
- Stevens RL, Fox CC, Lichtenstein LM, Austen KF: Identification of chondroitin sulfate E proteoglycans and heparin proteoglycans in the secretory granules of human lung mast cells. Proc. Natl. Acad. Sci., USA. 85, 2284-2287, 1988
- Maeda N, Ichihara-Tanaka K, Kimura T, Kadomatsu K, Muramatsu T, Noda M: A receptor-like protein-tyrosine phosphatase PTPζ RPTPβ binds a heparin-binding growth factor midkine. Involvement of arginine 78 of midkine in the high affinity binding to PTPζ. J. Biol. Chem., 274, 12474-12479, 1999
- Ueoka C, Kaneda N, Okazaki I, Nadanaka S, Muramatsu T, Sugahara K: Neuronal cell adhesion, mediated by the heparin-binding neuroregulatory factor midkine, is specifically inhibited by chondroitin sulfate E. Structural and functional implication of the over-sulfated chondroitin sulfate. J. Biol. Chem., 275, 37407-37413, 2000
- Zou P, Zou K, Muramatsu H, Ichihara-Tanaka K, Habuchi O, Ohtake S, Ikematsu S, Sakuma S, Muramatsu T: Glycosaminoglycan structures required for strong binding to midkine, a heparin binding growth factor. Glycobiology, in press.
- Kawashima H, Atarashi K, Hirose M, Hirose J, Yamada S, Sugahara K, Miyasaka M: Oversulfated chondroitin/dermatan sulfates containing GlcAβ1/IdoAaα1-3GalNAc(4,6-O-disulfate) interact with L- and P-selectin and chemokines. J. Biol. Chem., 277, 12921-12930, 2002
- Clement AM, Nadanaka S, Masayama K, Mandl C, Sugahara K, Faissner A: The DSD-1 carbohydrate epitope depends on sulfation, correlates with chondroitin sulfate D motifs, and is sufficient to promote neurite outgrowth. J. Biol. Chem., 273, 28444-28453, 1998
- Muramatsu T: Midkine (MK), the product of a retinoic acid responsive gene, and pleiotrophin constitute a new protein family regulating growth and differentiation. Int. J. Dev. Biol., 37, 183-188, 1993
- Muramatsu T: Midkine and pleiotrophin: two related proteins involved in development, survival, inflammation and tumorigenesis, J. Biochem.(Tokyo), 132, 359-371, 2002
- Iwasaki W, Nagata K, Hatanaka H, Inui T, Kimura T, Muramatsu T, Yoshida K, Tasumi M, Inagaki F: Solution structure of midkine, a new heparin-binding growth factor. EMBO J. 16, 6936-6946,1997
- Kadomatsu K, Huang RP, Suganuma T, Murata F, Muramatsu T: A retinoic acid responsive gene MK found in the teratocarcinoma system is expressed in spatially and temporally controlled manner during mouse embryogenesis. J. Cell Biol., 110, 607-616, 1990
- Tsutsui J, Kadomatsu K, Matsubara S, Nakagawara A, Hamanoue M, Takao S, Shimazu H, Ohi Y, Muramatsu T: A new family of heparin-binding growth differentiation factors: increased midkine expression in Wilms' tumor and other human carcinomas. Cancer Res., 53, 1281-1285, 1993
- Horiba M, Kadomatsu K, Nakamura E, Muramatsu H, Ikematsu S, Sakuma S, Hayashi K, Yuzawa Y, Matsuo S, Kuzuya M, Kaname T, Hirai M, Saito H, Muramatsu T: Neointima formation in a restenosis model is suppressed in midkine-deficient mice. J. Clin. Invest., 105, 489-495, 2000
- Sato W, Kadomatsu K, Yuzawa Y, Muramatsu H, Hotta N, Matsuo S, Muramatsu T: Midkine is involved in neutrophil infiltration into the tubulointerstitium in ischemic renal injury. J. Immunol., 167, 3463-3469, 2001
- Takei Y, Kadomatsu K, Matsuo S, Itoh H, Nakazawa K, Kubota S, Muramatsu T: Antisense oligodeoxynucleotide targeted to midkine, a heparin-binding growth factor, suppresses tumorigenicity of mouse rectal carcinoma cells. Cancer Res., 61, 8486-8491, 2001
- Unoki K, Ohba N, Arimura H, Muramatsu H, Muramatsu T: Rescue of photoreceptors from the damaging effects of constant light by midkine, a retinoic acid- responsive gene product. Invest. Ophthalmol. Vis. Sci., 35, 4063-4068, 1994
- Yoshida Y, Ikematsu S, Moritoyo T, Goto M, Tsutsui J, Sakuma S, Osame M, Muramastu T: Intraventricular administration of the neurotrophic factor midkine ameliorates hippocampal delayed neuronal death following transient forebrain ischemia in gerbils. Brain Res., 894, 46-55, 2001
- Ikeda S, Ichihara-Tanaka K, Azuma T, Muramatsu T, Yamada M: Effects of midkine during in vitro maturation of bovine oocytes on subsequent developmental competence. Biol. Reprod., 63, 1067-1074, 2000
- Muramatsu H, Zou K, Sakaguchi N, Ikematsu S, Sakuma S, Muramatsu T: LDL-receptor related protein as a component of the midkine receptor. Biochem. Biophys. Res. Commun., 270, 936-941, 2000
- Stoica GE, Kuo A, Powers C, Bowden ET, Sale EB, Riegel AT, Wellstein A: Midkine binds to anaplastic lymphoma kinase (ALK) and acts as a growth factor for different cell types. J. Biol. Chem., 277, 35990-35998, 2002
- Owada K, Sanjo N, Kobayashi T, Mizusawa H, Muramatsu H, Muramatsu T, Michikawa M: Midkine inhibits caspase-dependent apoptosis via the activation of mitogen-activated protein kinase and phosphatidylinositol 3-kinase in cultured neurons. J. Neurochem., 73, 2084-2092, 1999
- Qi M, Ikematsu S, Maeda N, Ichihara-Tanaka K, Sakuma S, Noda M, Muramatsu T, Kadomatsu K: Haptotactic migration induced by midkine: involvement of protein-tyrosine phosphatase ζ mitogen-activated protein kinase, and phosphatidylinositol 3-kinase. J. Biol. Chem., 276, 15868-15875, 2001
- Sakaguchi N, Muramatsu H, Ichihara-Tanaka K, Maeda N, Noda M, Yamamoto T, Michikawa M, Ikematsu S, Sakuma S, Muramatsu T: Receptor-type protein tyrosine phosphatase ζ as a component of the signaling receptor complex for midkine-dependent survival of embryonic neurons. Neurosci. Res., in press.
- Zou K, Muramatsu H, Ikematsu S, Sakuma S, Salama RH, Shimomura T, Kimata K, Muramatsu T: A heparin-binding growth factor, midkine, binds to a chondroitin sulfate proteoglycan PG-M/vesican. Eur. J. Biochem., 267, 4046-4053, 2000
- Kaneda N, Talukder AH, Nishiyama H, Koizumi S, Muramatsu T.: Midkine, a heparin-binding growth/differentiation factor, exhibits nerve cell adhesion and guidance activity for neurite outgrowth in vitro. J. Biochem(Tokyo)., 119, 1150-1156, 1996
- Kinoshita A, Yamada S, Haslam SM, Morris HR, Dell A, Sugahara K: Novel tetrasaccharides isolated from squid cartilage chondroitin sulfate E contain unusual sulfated disaccharide units GlcA(3-O-sulfate)β1-3GalNAc(6-O-sulfate) or GlcA(3-O-sulfate) β1-3GalNAc. J. Biol. Chem., 272,19656-19665, 1997
- Ohtake S, Ito Y, Fukuta M, Habuchi O: Human N-acetylgalactosamine 4-sulfate 6-O-sulfotransferase cDNA is related to human B cell recombination activating gene-associated gene. J. Biol. Chem., 276, 43894-43900, 2001
- Kaneda N, Talukder AH, Ishihara M, Hara S, Yoshida K, Muramatsu T: Structural characteristics of heparin-like domain required for interaction of midkine with embryonic neurons. Biochem. Biophys. Res. Commun., 220, 108-112, 1996
- Deepa SS, Umehara Y, Higashiyama S, Itoh N, Sugahara K: Specific molecular interactions of oversulfated chondroitin sulfate E with various heparin-binding growth factors: implications as a physiological binding partner in the brain and other tissues. J. Biol Chem., 277, 43707-43716, 2002
- Uchimura K, Kadomatsu K, Nishimura H, Muramatsu H, Nakamura E, Kurosawa N, Habuchi O, El-Fasakhany FM, Yoshikai Y, Muramatsu T: Functional analysis of the chondoroitin 6-sulfotransferase gene in relation to lymphocyte subpopulation, brain development, and oversulfated chondroitin sulfates. J. Biol. Chem., 277, 1443-1450, 2002




