
John Sheehan博士はイギリスのBristol大学で1970年に材料科学の理学修士号を、1973年に生物物理学の博士号を取得した。研究テーマはヒアルロン酸およびその他のグリコサミノグリカンのX線繊維回折であった。この研究が生物学における材料科学および物理学の応用に対して興味をもつきっかけとなり、彼はこの分野の研究を続け、糖質、複雑な複合糖質の構造が果たす役割について解明した。1979年にはPurdue大学で、1980-82年にはスウェーデンのLund大学でvisiting scientistとしてDrs. Heinegård , Lars Åke Fransson, Ingemar Carlstedtらとともにプロテオグリカンおよびムチンの構造と性質を研究した。以来彼は肺粘膜の防御機構に特に興味を持ち、最初はLancaster大学で、次いでManchester大学でWellcome Senior Lecturer and Reader(講師)としてヒトムチンの生化学および生物物理学の研究にほとんどの時間を費やして来た。1993年以降、彼は生物学における水の役割、特に多糖と糖タンパクにおける構造と動力学における水の役割に非常に興味を強くしている。2002年には、North Carolina大学の生物物理学および生化学の教授に就任することになっている。

Andrew Almond博士は1994年、Edinburgh大学で物理学の学位を得たのち、Manchester大学School of Biological Sciencesの博士コースに入った。彼の博士論文は、糖鎖と水の相互作用を実験的および理論的に研究することが中心で、ヒアルロン酸に力点が置かれていた。1997年Ph.D.取得後、1999年までManchester大学のWellcome Trust prize travelling research fellowとしてさらに他の多糖およびオリゴ糖の研究へと拡げていった。その後、Wellcome Trust prize客員研究員としてデンマークのCarlsberg研究所に移り、Klaus Bock教授の下でNMRを用いた、オリゴ糖の動力学的立体配置を知るための新たな実験的アプローチに取り組んだ。2001年、彼はイギリスに戻ってOxford大学でヒアルロン酸−タンパクの相互作用の分子モデリングを中心に研究をするためにTony Dayのグループに加わった。
ヒアルロン酸(以下HAと略記)は、単純な直鎖状のグリコサミノグリカンであり、一般的に多くの動物組織に高い分子量で存在する。これまでの20年の間に、HAに対する科学的な捉え方は、特定の細胞外空間を埋めるただの詰め綿的分子から、むしろ多くのマトリックス高分子が組織化される中心分子とする考えに変わってきた。大変広い範囲の生物学的機能がこの分子に負わされており、それゆえ、HAは多くの生理学的、臨床的および診断学的事象に重要な意味を持つ。またその構造的単純さ、分子量分布の広さおよび合成方式のユニークさにより、特有の進化的重要性を持つ分子として特徴づけられる1 。現在まで、天然でアセチル化、硫酸化またその他の修飾を受けたHAは見つかっておらず、この意味でこの分子は「完璧」である。このことと上に概略を述べた性質と相まって、生物学的機能の基礎となっている、と我々は提案する。
HAは多くの役割を果たしている。少量で十分である場合もあれば(例:軟骨におけるプロテオグリカンの形成役)、一方では主要な構造体であることもある(例:硝子体、Whartonさい帯ゼリー、または関節液)。したがってHAの機能は、その相互作用が主にタンパク質との間における三次および四次の組織化によるものか、または水およびイオンと粘性の高い溶液またはゲルを作るかによって大きく変化するようだ。生化学者および生物学者として、われわれは一般的にその機能と性質についてどちらかというと定位的な見方をしており、これら2つの世界を一つに融合することに困難を感ずる。特に半希釈と濃縮状態の溶液の各性質をいかに考えるべきかという議論がある2-4 。このレビューの目的は、この分子の動的な性質を考察することであり、またそうすることによりいくつかの一見矛盾した事象に対して説明の提案をすることである。
HAの固相におけるX線回折よりもさらに静的な観察はあまりない。1970-1985にかけて、異なる塩形態のHAの、半水和繊維あるいはフィルムを引き伸ばしたものを対象に多くのX線繊維回折研究がなされた。およそ6種の異なったバックボーン構造が観察され、これらのそれぞれは色々な充填配置に捕捉することができた。これらの構造のうち約8つについては、さらに詳細なX線解析が行われた。HAのカリウム塩について得た3つの異なった回折パターンで示されたように、一般的にデータの質は良かった(Fig.1)。回折パターンをさらに詳しく解析すると、糖鎖の優先的コンフォーメーションや、分子パッキング、それにイオンと水の協調関係についての洞察が得られた5-7。 これらの状態の起源、実験的にそれらがいかに互いに関連しているかについては、Sheehanらにより要約された8。 HA鎖は一般的に広がった2回軸、3回軸および4回軸のらせん構造をとっている。しかしながら、水の「構造破壊」イオン(低い pHにおけるNH4+、Cs+、Rb+およびK+)との共存下では、アンチパラレルの絡み合う二重らせん構造が見いだされた9。
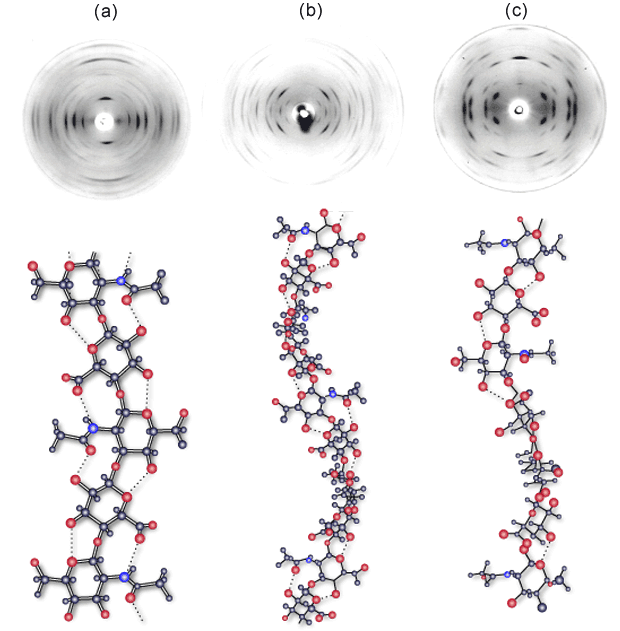
Fig. 1 HAカリウムのX線繊維回折
pH 2.0 (a), pH 3-4.5 (b)およびpH 5-8 (c)条件下でのHAカリウムの繊維回折パターン。(a)におけるX線繊維回折は、2糖あたり軸高0.98 nmの伸びた2回軸らせん構造と一致した。しかし詳細構造は不明である。(b)における回折は2糖あたり軸高0.84 nmの4回軸左巻きらせん構造と一致した。この湾曲した鎖は、正方晶ユニットセル内でアンチパラレルの二重らせんとして組織化されている9。(c)における回折は、2糖あたり軸高0.95 nmの広がった左巻きの4回軸らせん構造と一致した。これらの鎖の内の2つは正方晶ユニットセルにパッキングされている6。
われわれはこれらのデータをどのように見るべきか、そしてこれらのデータは、溶液中のHAの取りうる状態について、我々に何を示しているのであろうか?実験上、これらのデータは、HA水溶液の塩濃度とpHを必要条件に合わせてから、脱水して薄いフィルムを形成することにより得られる。このフィルムを次に細長く切り、ポリマー鎖の方向性をだすために高湿のもとで伸ばした。時間の経過とともに(数日から数週間)ポリマー鎖が形成され、結晶化する。この手順により、ポリマー鎖が形成されて優先的低エネルギーコンフォーメーションの配置にパッキングされる。しかしながら、これらの配置の特殊性とその数は驚きであった。このことより、HAのコンフォーメーションは柔軟で、糖鎖の周囲の水と陽イオンの配置に非常に左右されやすいことを示唆している。重要なのは、X線繊維回折は、HA鎖がとりうるコンフォーメーションのうちの一部の構造しか捉えることしかできず、今回の配向の結果は、HA分子がほかの可能とされる安定的なコンフォーメーションに逆らって選んだのではと、想起させられることも心にとめておく必要がある。
興味深いことに、コンフォーメーション間で多くの遷移が固体状態において観察された。特に面白いのはカルシウムの効果であり、HAナトリウム繊維を塩化カルシウムで洗うと、らせんコンフォーメーションが4回軸から3回軸に変化した8 。そして、HAナトリウム溶液を少量のカルシウムで滴定すると、その粘性、沈降および拡散の性状にもはっきりとした変化がみられた3,10 。これらのデータは、このイオンの存在下でポリマーの動力学に変化が生じたことを強く示唆している。配向した繊維とフィルムを希酸溶液で処理しても、3回軸または4回軸のコンフォーメーションから、2糖当たり0.98 nmの軸高をもった、広がった2回軸のコンフォーメーションを示す回折パターンへと変化した(Fig. 1a)。このパターンが固有の構造として指し示されたことがないのは、おそらく2回軸のコンフォーメーション配置が縮退し、一本の繊維中に複数のらせん構造が共存する状態を引き起こすためであると思われる。このコンフォーメーションは、pH 3.0以上では不安定であり、共存する陽イオンによりさまざまな3回軸または4回軸のコンフォーメーションにとって替わられる。
以上のデータから得られる一般的結論は、HAは溶液中で非常に活動的で、特定のイオン条件に対して敏感であり、これにより大容量の溶媒中では変化を起こし、結晶格子中のイオンとの配位が特に必要になってくる。しかしながら、詳しく研究された全ての充填配置において、左巻きらせんが非常に優先的であること、近距離間の水素結合は常にアンチパラレル鎖との間に見られることは興味深いことである。
分子量と溶液中の分子のサイズの関係を計測することは、溶液中でのその分子の「平均的」な形状を知る上で有用な指標である。HAの流体力学的研究は長年にわたっておこなわれてきた。最近、純粋な試薬HAが入手可能になったことにより、広範囲の条件下における溶液中の性質を解明する多くの研究がなされるようになった。おのずとHA分子の固さの程度が議論の的となっている。分子内および分子間の水素結合と疎水結合相互作用2,3が、その溶液中の性質にどの程度寄与しているのかについても同様である。
共通した見解は、HAは非常に高濃度に至るまで、その濃度と分子サイズに依存して粘弾性溶液またはペーストの状態を維持することである。それは、決して固体のゲルを形成しない、すなわちHA溶液はある種の架橋剤を加えない限り、真に粘弾性を、また急速なアニーリングを示す。その分子構造の規則性だけでなく、X線回折データから証明された高い組織性と密な充填構造を考慮すると、これはある意味で予測外である。われわれは直感的にHA分子鎖がアガロース、カラゲナンそれにアルギン酸ゲルに提案されたものと類似した方法で充填し、積み重なることによって、同じような固いゲルを形成すると感じる。
希薄溶液において、HAは固いランダムコイルで、分子鎖は特別な相互作用をほとんど、全く見せないと一般的に考えられている。そのような条件下での、persistence lengthの長さには議論があるところだが、現在の評価では4-8 nmと考えられる11。分子鎖同士が重なり合う濃度では、動粘度に変化が見られる。しかしながら、最近の半希釈濃度法による研究では、中のHA分子は、互いにからみあった分子鎖の動的ネットワークが最適なモデルであると示している3。
文献上では、HAの多くの生物学的性質はその分子サイズに左右されるという報告がいくつかなされている。われわれは最近の研究で12、希薄溶液中でHA分子の流体力学的挙動は分子サイズに依存して変化するかどうかを調べた。我々は4糖から12糖までのサイズのHAをイオン交換クロマトグラフィーで、また分子量5,000から100,000までをゲルクロマトグラフィーで単離した。希薄溶液中での拡散係数の測定は、流体力学的サイズの直接量を提供し、オリゴ糖に対してはTaylor13によって考案され、最近になって改変された分散技術法12により測定された。この方法は、パルス投入された溶質分子が毛管内を層流として流れる際の拡散効果に依存しており、非常に高感度、高精度におこなうことができる。オリゴ糖は、分子が伸展した環状シリンダーとしてモデル化された。HA分子の質量/長さの比と一致して大きく伸展した構造が動力学的モデルとX線回折で見られる。得られたデータは4糖以上のオリゴ糖モデルと見事に一致した(Fig. 2a)。
広い範囲の、特別に分画した高分子量HAの拡散係数を測定するために動的光散乱の手法が用いられ、同時に得られたデータも集められた。これらの実験は、pH 6.0(Fig. 2b)(HAが高分子電解質である場合)と、pH 2.0(Fig. 2c)(荷電的に中性高分子である場合)の条件下でおこなわれた。低分子量においては、分子量とサイズの関係(曲線の傾きから得られる)は、極めて硬くほとんど棒状の分子鎖と一致した(Fig. 2b、c)一方で、Mr 10,000以上では分子の挙動は、はっきり変化し、分子量が増加するにつれコイル状になった。この挙動は、静電気的相互作用効果が抑制されるpH 2.0で特に顕著だった。われわれは、糖鎖が長くなればなるほど、よりランダムコイルとしてふるまうことは予測していたが、棒状からコイル状への遷移領域が比較的低分子領域にあることは予測しなかった。
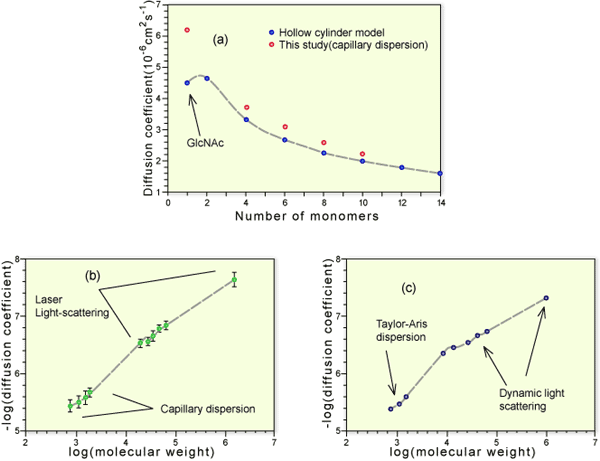
Fig. 2 HAの分子サイズと分子量の関係
HAオリゴ糖はゲルクロマトグラフィーとイオン交換クロマトグラフィーで分離した。オリゴ糖の拡散係数は、キャピラリ分散法(a)(白丸) で測定し、適切な質量/長さの中空円柱モデルをベースに計算した値と比較した(a)(黒丸)。より大きな高分子はゲルクロマトグラフィーで分離し、分子量はオンライン多角度光散乱で、拡散係数は準弾性光散乱で測定した。測定された分子量と拡散係数はlog-logスケールでプロットした。(b) 0.2 M NaCl、pH 6.0の結果、(c) 0.2 M NaCl、pH 2.0の結果。どちらの条件でも初期勾配は棒状構造と一致した。しかしながら分子量10,000以上での勾配は固いランダムコイルに一致した。この遷移は特にpH 2.0で行われた実験で顕著であった。
希薄溶液の条件下で、このような著しい遷移はいかにして起こるのだろうか?2糖の最も伸びた長さを1 nmとすると、先の分子量依存性から、鎖長が25 nmを越えるとその性質に変化が生じることが示唆される。われわれは、この変化について確たる説明ができない。現在研究中であるが、推測の一つは、この長さ以下のHA鎖は分子内セグメント間の相互作用をまったくもてず、一方でこれ以上になると、HA鎖が集合することで自己相互作用の構造が生まれる可能性があり、そのため通常よりもその平均的なサイズが小さいからではないかと考えている。
すべての生体分子と同様に、HAの分子的性質は水との相互作用から生まれる。最近まで、分子内相互作用に比べ、これらの相互作用とその持続性については余り知識がなかった。現代のコンピューターによるアプローチにより、今では水分子の存在下における、これらの分子断片の実際的な動的シミュレーションが可能となった。ジメチルスルホキシド中のオリゴ糖のNMR研究では、特異的水素結合の存在を同定できるが14 、水溶液中では各水素結合は観察できなかった15 。これらのデータから、こうした結合は水との動的相互作用の中にあることを示唆するが、ドメインの関与した時間や、結合の平均的な特性に関する確実な情報は得られない。
われわれは、HA鎖がどのようにそのコンフォーメーションの空間を取るのか、またもしあるとすれば、分子内水素結合がHA分子の安定性において何の役割を果たしているかの手がかりを得るために、2糖、4糖および10糖についての分子動力学上の計算を行った16-18。 Fig. 3は、4糖が1,000個の水分子を含んだボックスに入れられた、動的状態を示している。曲がりやすいグリカンに対して、水の水素結合の活性がいかに優勢であるかは明白である。われわれがおこなった分析の特性を強調できるよう、10糖のシミュレーションから得たデータをここに示す。
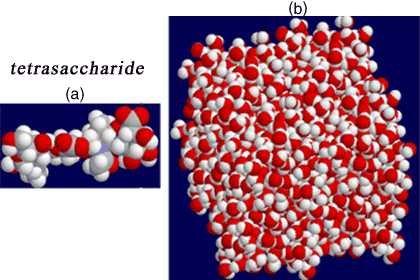
Fig. 3 HAオリゴ糖の分子動力学
2糖、4糖 (a)、10糖構造のモデルを作成し、300 Kに平衡化させたTIP3P水分子で満たした適切な「周期」ボックスに置いた(b)。シミュレーションは5ナノ秒に至るまで行い、座標は1フェムト秒間隔で更新させた。すべての空間座標は解析に利用できるので、時間経過におけるコンフォーメーションの動きが詳細に調べられる。
φ(ファイ)とψ(プサイ)のねじれ角度はH1-C1-Ox-CxとC1-Cx-Cx-Hxとそれぞれ定義した。 β1-3結合ではx=3、β1-4結合ではx=4である。100 fs毎にサンプリングしたグリコシド結合を規定するφとψ角度の値をFig. 4に示した。このグラフにおける各ポイントの密度は、そのコンフォーメーションが見いだされる確率を示しており、このシミュレーションでβ1-3結合には1つのコンフォーメーションが優勢であることがはっきりとわかる一方で、β1-4結合には複数の可能性が見られ、すなわち、いくつかの結合では少なくとも2つの異なった優勢領域が見られている。このようなコンフォーメーションはどのようにして抽出されるのであろうか?この質問には各結合につき、時間軸とともにψとφ角度を記録することにより答えられるであろう。我々はFig. 5で1つのβ1-4結合についてこれを示した。コンフォーメーションはナノ秒という時間で1つの極小範囲内を変動するが、わずか2-3ピコ秒間にジャンプを完了して他のレベルへ迅速に遷移している。
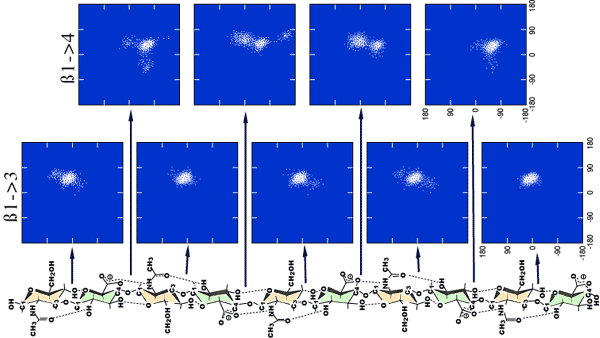
Fig. 4 HA10糖水溶液シミュレーションでの各グリコシド結合角度
各グリコシド結合の φ / ψ 角度は、5ナノ秒間を通して100フェムト秒毎に出力した。各ポイントの密度は、その空間配置を取る分子の見つかる確率とそのエネルギーを反映している。β1-3結合は1つの点が優勢であるが、β1-4結合周辺の動的空間は多様な状態を示し2つの明瞭な領域が現れている。また、β1-4結合の末端1つ手前では「末端」効果も見られる。
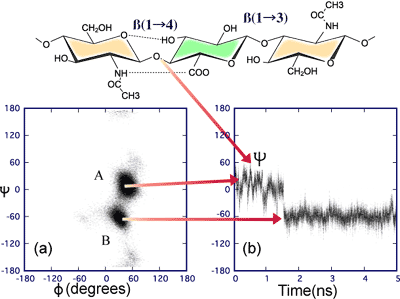
Fig. 5 β(1-4)結合におけるψ角度の時間変化
10糖の5ナノ秒間シミュレーションにおけるβ1-4結合の、φとψ角度を100フェムト秒毎に抽出した結果を(a)に示した。ここでは2つの動力学的に優勢な状態の存在が示されている。経時的にグリコシド結合角を追うと、ナノ秒単位でのψ角度の急激な変動によって分子がどのようにして状態AからBへジャンプするかがわかる(b)。しかしながらジャンプが起きるのはピコ秒単位である。
シミュレーションの進行過程で生じる分子内水素結合は、10糖分子がいかに早くコンフォーメーション空間を占有するかを測定する、ひとつの指標ともとれる(Fig. 6a)。これらのデータは、利用できる優勢な自己相互作用のほとんどは、シミュレーションにおいて2-3ナノ秒以内に現れていたことを示している。これらの水素結合を分析した結果、β1-3結合でのAとBは非常に持続的だが、β1-4結合ではC、D、EおよびFが大変重要であることが示唆された(Fig. 6b)。ヒドロキシルメチル基の役割は、HAのコンフォーメーション研究では注目されてこなかったが(E、F)、我々の全てのシミュレーション研究によると、これはHAの動力学において重要な役割を担っていることが示された。
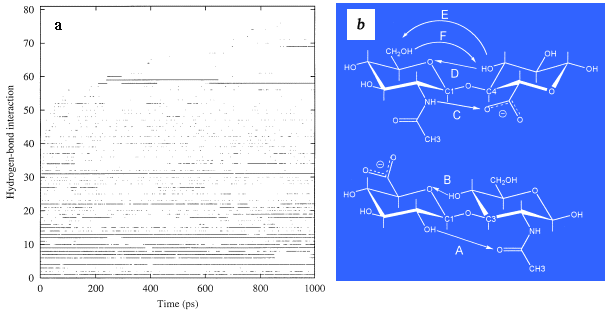
Fig. 6 分子内水素結合の生じる時間経過
100フェムト秒間以上続くHA分子内の持続する水酸基アラインメントを、分子内水素結合の指標とした。このような相互作用の発生は、シミュレーションを通して時間関数として表され、そのような相互作用すべては2-3ピコ秒内にサンプリングされたことがわかる(a)。最も持続的な水素結合はグリコシド結合で生じるものであり、β1-3結合ではAとB、β1-4結合ではC、D、E、Fである (b)。これらの結合の時間関数的サンプリング結果はFig. 7に示した。
全体としてX線回折データは、HAが水および陽イオンの環境に対してきわめて感受性が高いことを示している。調べられたコンフォーメーションはいずれも全て伸展していて(即ち2糖当たりの軸方向の長さは0.84から0.98 nmの変化を示す)、さらにこれらは左巻きらせんへの強い優先性を示す。これらの性質は、分子動力学の計算から得た予測と完全に一致する。分子量10,000までのHAナトリウムは、溶液中ではX線回折の解析値と分子動力学による予測値から得られた結果に類似した局所平均ディメンションをもつ、大きく広がった構造をとるモデルとなりうることが明白である。伸展した状態をとろうとする一般的傾向は、動力学的シミュレーション(Fig. 7)を通しても見られるが、ここでは末端間の距離の変動から完全に伸展した状態に戻ろうとする傾向を示す。このように、これらの多くの低エネルギー状態は、イオン−水−糖鎖の協調関係と同様に対称性および糖鎖のパッキング限定性と一致しなければならない。しかしながら、上記討論から、HAが溶液状態で長期にわたって特異的コンフォーメーションを保持しているということを推論すべきではない。HAは迅速に相互転換する複数のコンフォーメーション状態のセットであり、その内のいくつかは顕著なねじれ効果を示し、また非常に短い時間内で末端間距離を短縮するということが、動力学から明白になっている。
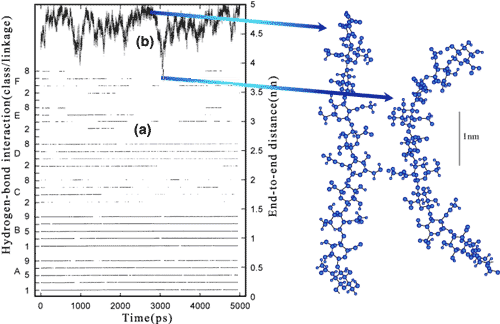
Fig. 7 HA10糖の主要グリコシド水素結合の時間変動と末端間の距離
β1-4結合の水素結合A、B、C、Dとβ1-3結合の同じくEとFを、時間関数的に表した(a)。AとBは特に持続性があるが、一方CとD間では急激な交換があることがわかる。HA10糖の伸びきった長さは4.95 nmであり(b)、分子はこの状態に移行する傾向があるが、より収縮した状態への急激な変動がある。右図はシミュレーション中にサンプリングした伸びた空間配置(c)と収縮した空間配置(d)の例である。
周辺水分子との水素結合の形成に対して、分子内水素結合の役割をわれわれはどのように考察すべきか、との疑問が生じる。広がったコンフォーメーションは、確かに前に述べられた(A、B、C、D、E、F)ような、分子内水素結合が存在することを示しており、それらはすべて広がったコンフォーメーションと調和する。水素結合は、分子を「固くするもの」と解釈すべきであろうか?われわれの回答は多分に否定的である。
一般的に分子の水素結合の相手が自身であれ、水分子であれ、水素結合エネルギーにほとんど差はない。われわれは以前にシミュレーションの詳細な結果をもって、分子の動力学的変化を緩やかにし、かつ分子内水素結合を促進させている水分子が、逆説的であるにもかかわらず、立体構造間の急激な変換も促していることを示した。立体構造状態間の迅速なジャンプは、時折グリコシド結合の周囲に捕捉され、エネルギーをHAに送る水分子を介して、触媒される。
動的水分子の集団と接触した固定水分子は、生体分子とその直近の水分子に対して強制される配列が原因で、エントロピー的に非常に不利である。こうして平均的に見ると、HAは動的な水構造に対するヒドロキシル、カルボキシル、およびN-アセチルアミド側鎖グループの、妨害が最少となる状態と一致する方向に押し出される。生体分子の全てのクラスにおけるそのような状態は、しばしば分子内水素結合の存在と一致することが頻繁に観察されるが、この水素結合はもちろん静電気を「包んで」いる。この観点から、我々はHAの多くの広がったコンフォーメーションが、HAプラス水における最大エントロピーと強く一致することを主張したい。
上述してきたように、動力学に関する詳細な本質は非常に興味をそそられる。HAは伸展した状態をとろうとする傾向をもつが、実際にはナノ秒の時間単位で交互に置き換わることができるいくつかの状態のアンサンブルを探っており、これらの状態の多くは、短いオリゴ糖においても、Fig. 7で焦点を当てたように、分子を強くねじれさせることができる。特にβ1-4結合の動力学では、いくつかの異なった状態間で迅速に変換することを示し、このためこの分子はコンフォーメーション的に不安定となっている。この絶え間ない動きこそが、この分子の自由な溶液特性の理由となっているというのが我々の推論である。特筆すべきは、鎖間の長期にわたる静的会合の形成を阻害することで、HAの粘弾性を保持し、高濃度にあっても静的ネットワーク構造の形成に対抗する。この迅速な動力学的コンフォーメーションの相互変換速度は、HA溶液の動力学的および伸展性流動特性に重大な影響を与え、また、多くの重要な生理的特性の基礎となっているのであろう。
Colemanらの研究は19、HAは、滑膜を流れる圧力/流れに誘導された浸透圧流の制御に重要な役割を演じていることを示しているが、その一方で伸長流においてエネルギーを吸収する性質は、体のおもな関節部位で生じる迅速な動力学的衝撃下での、エネルギー散逸におそらく不可欠である。また上述してきた動力学的特性から、HAを完全なる「空間」とする分子と推測することもできる。HAの形状変化のナノ秒の動力学は、すき間を埋め、表面に適応し、そしてもし優先的伸展状態が阻害された時には、それに逆らう力を発生させる。このような働きは、創傷治癒や分化の過程での細胞運動に重要であると思われる。
上述してきたように、われわれはHAの動力学の機能的重要性を強調してきた。しかしながら、その挙動には自己類似性と柔軟性が重視されるべき、ほかの側面もある。これらの特性が、タンパク質との協同的相互作用に基づく安定した構造複合体を構築する上で完璧な環境をつくる。細胞外マトリックス中の多くの環境下で、異なったHA−タンパク繊維複合体が非常に接近して見いだされることは明白である20。報告されている証拠を総合すると、一般にはこれらの複合体は細胞の外側で形成されることが示唆されており、質量作用の法則から考えて、それらは幾分多様であることが予測される。これが観察されていないのは、おそらくHAがその上で異なったタンパク質が結合するa、多くのさまざまな形をした土台を提供するためと考えられる。例えば種々のタンパク質が、全て同等のエネルギーをもった、種々のコイル状や伸展した形状にHAを引き込むことができる。これらの推察は多くの研究グループにより追試されている過程にあり、近い将来には多くの知見が得られることになろう。
a 本シリーズのDayの総説参照
我々は、HAの極微レベルの行動に関する見解を述べてきた。この見解は、この単純な分子の溶液の観察可能な基本的性質は、わずかピコ秒(10-12秒)という時間的スケールの間に出現するという驚くべき提案(少なくとも我々にとって)に基づいている。それは、ナイフの刃先のような、秩序と混乱の境目に位置し、そこからあんなに多くの機能が現れている。この時間スケールでHAを直接測定することは現在のところできないが、しかしここ数年の内にはそのようなことが可能になるだろう。このようにHAの溶液特性への理解を深めることは、この新しい世紀に入ってもなお、われわれに課せられた知的賦課であると考える。