
谷口 直之 教授
昭和42年北海道大学医学部卒、昭和47年同大学院医学研究科修了、医学博士、昭和50年同大学医学部衛生学講師、昭和51年から52年コーネル大学医学部生化学客員助教授、昭和52年北海道大学院環境科学研究科助教授、昭和54年同大学医学部癌研生化学助教授、昭和61年大阪大学医学部生化学教授、平成7年〜アメリカ生化学/分子生物学会(ASBMB)名誉会員、糖質学会常任理事、平成10年〜文部省特定領域研究(A)「糖鎖リモデリングと細胞コミュニケーション」」領域代表者、2001年日本生化学会会頭、J. Biol. Chem., Glycobiology, Glycoconjugate J.などの 常任編集委員
ヒトゲノム全塩基配列決定の日が間近となり、疾病関連遺伝子の解明やゲノム創薬などへの応用に対する期待が高まっている。糖質科学の分野においても、近年糖鎖の合成に関わる多数の糖転移酵素の遺伝子がクローニングされ、その機能のシステマティックな解析も進められている。このような状況を背景に、今日の糖質科学研究の焦点は多様な糖鎖構造の意義やそれを合成する生体調節機構の解明へ向かいつつある。
日本における複合糖質研究は、長年文部省の研究班に集う研究者の活躍によって多くの成果をあげてきた。現在は「糖鎖リモデリングと細胞コミュニケーション」班がこの研究を継承し、課題に取り組んでいる。この領域代表者である谷口直之教授にご自身の研究の軌跡、最近の関心事および今後の糖質科学研究の課題などについてお考えを伺った。
Q先生はどのような経緯で糖の研究に入られたのですか?
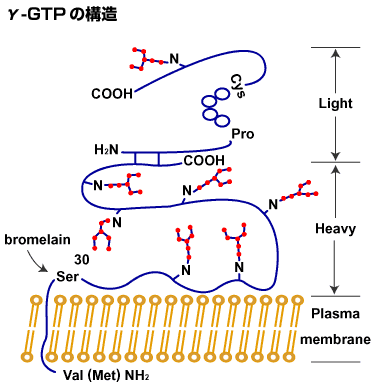
私は北大大学院で最初含硫化合物のケミストリーのテーマをいただき、その代表的物質であるグルタチオンの研究に入りました。グルタチオンは酸化・還元で最も大事な低分子化合物ですが、それを分解する酵素、γ−グルタミルトランスペチダーゼ(γ-GTP)の分離と精製が私の学位論文でした。その後、コーネル大学医学部のマイスター教授および北大がん研の牧田教授のところで、このテーマを続けて、γ-GTPのがん性変化、そのエンザイマティックなメカニズムの研究などを中心にやっておりました。
Qこのγ-GTPが糖蛋白だったわけですね。
胎仔やがん細胞から精製したγ-GTPの糖鎖には、いろんなヘテロジェニティーがあるということがわかったのですが、当時は私のところで糖鎖を解析する力がありませんでした。ちょうどその頃、γ-GTP糖鎖に興味をもたれた木幡教授(当時神戸大)からの誘いで共同研究することになり、そこにバイセクティングGlcNAcを見いだしたというのが、現在の研究に入ったきっかけでしょうね。 その後、大阪大学に移ってから、このバイセクティングGlcNAcをつくるN-アセチルグルコサミン転移酵素(GnT)、 GnT-IIIの活性測定法を開発し、酵素の精製、cDNAクローニング、遺伝子クローニングというふうに進んできたわけです。
Qそのγ-GTP糖鎖の研究はどのように進んだのですか?
γ-GTPの糖鎖は主としてコンプレックスタイプなんですが、ネズミでは肝がんからとったものだけにバイセクティングGlcNAcが多く、正常ではほとんどないことがわかりました。がんになるとGnT-III活性が肝臓で100倍ぐらい増えます。この酵素は正常の肝臓にはないんですが、腎臓には一番多い。そこで、ネズミの腎臓からこの酵素の精製をはじめたのですが、分離精製に3年ぐらいかかりましたね。 それから糖転移酵素の遺伝子クローニングに成功しました。GnT-IIIの次にGnT-Vをクローニングしましたが、これはほんの1カ月ぐらいのちがいで他のグループが先行しておりました。しかし、私たちはヒトの組織からも全く独立して同じ酵素をとり、遺伝子のクローニングも成功しました。
これに次いでα-1,6のフコシルトランスフェラーゼ(FucT)という、αフェトプロテイン(AFP)の根本の2つのGlcNAcのところにフコースを転移する酵素を精製しました。 AFPというのは、肝がんになると増えるんです。しかし、急性肝炎や肝硬変などのときも、血液の中に出てきます。だから、腫瘍マーカーとしてもちろん有用ですが、診断率は6割5分から7割位程度でしょうか。 ところが、α-1,6のフコースのついたAFPというのは、肝がんにかなり特異的なんです。そこでα-1,6のフコシルの機構を知るのは面白いということで、α-1,6FucTもヒトの胃ガン細胞とブタの脳から精製して遺伝子クローニングをしました。
がんでは糖鎖のわりと枝分かれのところに異常が起こるので、その酵素にわれわれは興味を持っています。すなわち、興味のすべてに枝分かれが関わっているんです。 以上の研究では、私たちはいわゆるESTを使ったホモロジークローニングというのは一切していませんで、すべて蛋白をとってその性質を見て、それから遺伝子クローニングをやろうというストラテジーでやっています。
QGnTにはいろいろあるようですが、その意義はどういうことでしょうか?
そうですね。GnT-Iというのは、ノックアウトすると死んじゃいます。ただ、枝分かれ糖鎖を作るGnTにIII、IV、VとかVIというのもあるんですが、これらのGnTにはお互いにホモロジーがなくて、そういう意味では、むしろ新しい遺伝子なんですね。つまり、どんな動物でも持っているわけではなく、イーストにはないけれど線虫なんかには一部持っているというように。
糖鎖遺伝子というのは臓器や組織または細胞によって、それぞれ全くスペシフィックに発現するわけですね。ですから、たぶんがんのときや、腎臓のとき、脳のときというのは、全く意味が違う働きを持っていると思います。 β-1,6Gn糖鎖はがん転移に関わっていますので、この糖鎖を合成するGnT-Vは悪玉と考えられますが、GnT-IIIはバイセクティングGlcNAcをつくってβ-1,6Gnの生成を抑えるので善玉であるというふうに言えます。ただ、GnT-IIIを過剰発現させたトランスジェックマウスでは、リピッドの蓄積が生じ脂肪肝ができるなど、新しい病気をつくる可能性がありますから、この場合は善玉とは言えないんです。 GnT-IIIがほかの組織に発現されたときは、それがどうなるかというのはちょっとまだわかりません。そのほか、脾臓のNK細胞に対する感受性を抑えてしまうとか、α-1,6FucTを過剰発現するとウオルマン病という、やはり脂肪が蓄積する病気になるなどいろんなことを見つけています。 ですから、糖鎖遺伝子というのは、その組織、あるいは細胞によってその機能はかなり違って、その意義も違うんじゃないかというふうに思っています。
Qこれらの酵素の遺伝子の場所、その発現の調節はどうなっているのでしょうか?
GnT-III、IV、V、α-1,6FucTは染色体の位置が全部違うところにあります。 何か病気につながるのかもしれませんが、今のところ全くわかりません。機能も全く別で、かなり早い時期に分かれてしまっているんだと思います。
糖鎖遺伝子一般にそうですけれども、現在、遺伝子の調節機構がわかっているのはGalTの一部だけですね。 GnT-IIIも残念ながら、なかなかどういう調節機構をやっているかまだよくわかっていないんです。
Qこれら糖転移酵素の蛋白構造はどの程度分かっているのでしょうか?
高次構造が少しずつわかってきましたね。例えばβ-1,4GalTとか。今度GnT-Iも結晶解析が出たんです。 GnT-III、Vは糖がついていますので、ちょっと結晶解析というのは難しいところがあります。α-1,6FucTは糖がついていないので、これはひょっとするとそのままでできるかもしれません。確かに糖転移酵素のドメイン構造はほとんど似ていますから、アクセプターを認識するところ、ドナーを認識するところの構造というのは、どんどんわかってくるでしょうね。だから、酵素反応としては、非常に理解が進むと思うんです。ただ、細胞の中、ゴルジの中でどういう局在をしてどういうクラスターをつくっているかという話は、なかなかまだもっと先じゃないとわからないでしょうね。
Q作られた糖鎖の役割についてはどうでしょうか?
セレクチンと相互作用する糖鎖はどんどんわかってきています。糖蛋白を認識する方では、もちろんC型レクチンというような糖鎖は若干ありますけれども、Nグリカンをスペシフィックに認識するリガンドというのはなかなか難しいです。結局、そういう特定の糖鎖を固相化して、それに結合する蛋白を追っかけていくか、あるいは例えばツーハイブリッドシステムみたいなのをうまく利用してやるかということしかないわけですね。
糖鎖を認識するレクチンがどういうところにあり、どういう性質を持っているのかというのは、まだほんとうにわかっているのは数少ない。例えばβ-1,6のブランチを持った構造というのは、転移性のがんにたくさん出てくるわけですけれども、どうしてそれをがん細胞が認識しているのかというのは全くまだわかりませんですね。そういうこともこれからやらなきゃならないと思ってはいるんです。
Q糖鎖遺伝子のノックアウトからのアプローチはどうでしょうか。
GnT-Vはノックアウトができまして、そのネズミはがんになりにくいということがわかっています。 GnT-Vの遺伝子を欠損したのはがんになりにくく、GnT-Vの遺伝子を注射してやるとがんができます。これはつまりGnT-Vは、オンコジンに近いわけですね。それから、GnT-IIIはあまりフェノタイプが出てきていないんですが、ノックアウトしてしまうと、肝化学発癌に対して抵抗性になるという話があるんですね。それは多分臓器によって違うんじゃないかと思うんですけど。だから、これもそういう意味では、両面性を持っていて、両刃の剣のような働きをしている可能性がありますね。
Q近年、沢山の糖鎖遺伝子がクローニングされましたが、これからの糖質研究の方向についてどうお考えですか?
先の糖鎖遺伝子研究班(斉藤班)では、とにかく糖鎖遺伝子を主力的にやろうということで、多くの遺伝子のクローニングを行いました。シアリルモチーフによるホモロジー・クローニングなどで大きな成果がありましたね。この班では糖鎖遺伝子をとにかくとって、キャラクタライズするというのが中心で、世界の糖鎖遺伝子の約7割ぐらいのクローニングに成功したと思います。しかし、バイオロジーはまだ一部で、これからという状態でしたね。
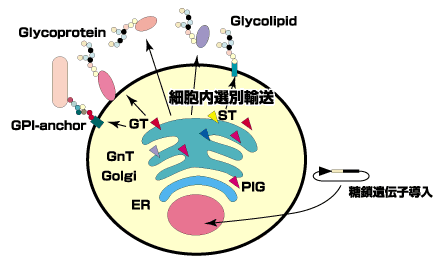
現在の私たちの研究班では何をねらったかというと、ほぼ手中にした遺伝子を細胞に導入して、個体、あるいは細胞がどうなるか、フェノタイプがどうなるか、それからもちろんノックアウトをしてどうなるかということですね。また、細胞間の特異的なリガンド、シアリルルイスエックス、ミッドカインやグロースファクターなど、プロテオグライカンとの相互作用とシグナルがどう行くかということ、こんなことを最初のプロポーザルで出しました。 すでに主なパブリケーションが約400編ほどあり、糖鎖合成遺伝子の単離・機能・同定でレベルの高い業績が出ていると考えています。あと1年半なんですけど、多分もう少し新しい仕事がまた出てくると思います。
Q糖鎖を作るには複数の糖鎖遺伝子が関与するので、蛋白の場合とは違って複雑ですね。ひとゲノム解読研究と比べてどのような意義があるのでしょうか?
まあ、糖鎖遺伝子と言えば、我々たまたま糖転移酵素を中心にしているので、それを全面的に出していますけど、実は糖鎖を分解する酵素の遺伝子やレクチンなど全部をほんとは含めるわけですね。
2003年までにヒト遺伝子がすべて同定されるということですが、遺伝子の解明それだけでは細胞生物学を理解することはまずほとんど不可能で、病気を理解し、治療するというところまでは至らないと思いますね。
人間の体、細胞というのは多様性に満ちていて、とてもそんな遺伝子1つだけで病気を論ずることは、多分できないと思います。
Qそういう多様性は、遺伝子のファンクションにあるということで、もう少し総括的に インテグレートしたプロテオームという概念が出てきたわけですが、それを糖鎖科学から見るとどうとらえたらよいのでしょうか?
プロテオーム研究では、2次元電気泳動で蛋白を同定して、その性質はどうだ、インタラクションはどうだということをやっています。じゃあ、プロテオームの多様性を決めているのは何かというと、やはり糖とか燐酸化とかが重要なポイントになると思います。 ですから、プロテオームに匹敵するグライコーム、プロテオミックスにあたるグライコミックスという概念があってもいいわけです。もうちょっと糖鎖生物学、糖鎖工学をインテグレートした形のものを、グライコミックスと呼ぼうということです。これは実は既に5年前に、アメリカのVernon Reinhold教授がこのテーゼを立てています。いわゆるポストトランスレーショナルモディフィケーションにグライコームという概念を当てはめてはどうかと。そういう技術を伴った学問をグライコミックスと言っていいんじゃないかということですね。
ある遺伝子をノックアウトしたら、特定の病気が起こり、因果関係は明らかになる。ところが、糖鎖の場合には、糖鎖遺伝子をノックアウトしても、それはダイレクトなものじゃなくて、間接的にほかの遺伝子がやられた終末像なんですね。糖鎖というのは、いろんなところのステップ、しかも最終段階に影響する糖蛋白、糖脂質、プロテオグライカンをモディファイしていますから、逆に言うと、非常に最下流の、病気が発症するところに最も近い現象を見る確率が高いと思うんです。だからむしろダイレクトなんです。そこをもうちょっと強調する必要があるなと、このごろよくいろんなところで考えていたんです。 病気の原因は非常に複雑であるけれども、ほんとうにその原因を規定しているのは最後の修飾であるわけです。だから、1遺伝子が1つの機能を持っているのではなくて、いろんな組み合わせがあってファンクションが出てきている。でも、糖鎖に関しては、ひょっとすると、そういうワンファンクションを規定している可能性があり、だから、むしろそちらが大事だというふうにこのごろ私は思っているんです。そこをグライコームの概念は包括しているんじゃないでしょうか。
私はいまブタからヒトへの異種移植の研究にも関与していますが、問題はブタには細胞表面にα-1,3Galエピトープ糖鎖があり、ヒトにはこのエピトープに対する自然抗体があるので、超急性期の拒絶反応が起こることです。この糖鎖を作るブタの遺伝子をノックアウトする技術はまだないんですね。しかし、GnT-IIIを使って糖鎖にバイセクティングGlcNAcを入れてやると、エピトープGalの合成がほとんどなくなることがわかりました。今、私はこの方法で何とかこのエピトープを機能的にノックアウトしようということをやっております。
こういった研究や現象の解明が増えてくれば、グライコームの概念がものすごく大事なものだと理解されてくるんじゃないかと期待しているんです。すでにC.elegansを使ってグライコームの分析が海外では始まっています。