|
糖化脂質の多様性と生体膜機能
|
 |
| (First version published: 2002年6月15日) | |
|
 |
生体膜脂質は、糖による修飾を受けることにより、多様な分子種を生む(1)。哺乳動物細胞膜に普遍的に存在する糖脂質のほとんどは疎水性のセラミドのグルコース化を触媒するグルコシルセラミド合成酵素(GlcT-1, UGCG) から合成されてくるスフィンゴ糖脂質(GSL)である。セラミドのガラクトシル化により合成されるガラクトシルセラミドは、ミエリン膜の特徴的な脂質として存在する。グリセロタイプの糖脂質は、組織特異的に存在する。例えば、精巣にはガラクトシルアルキルアシルグリセリド(セミノリピド)見いだされている(表 I)。グルクロン酸やグルコースで糖化されたコレステロールが、ヒトの肝臓や繊維芽細胞からそれぞれ単離されている。
|
|
|
| 表 I Roles of monoglycoslated lipids in mammals: most all lipids are glycosylated
. |
|
|
|
|
|
|
|
 |
|
|
|
|
|
|
|
| Glycolipid |
|
Distribution |
|
Synthetic enzyme |
|
Role |
|
|
|
|
|
|
|
 |
|
|
|
|
|
|
|
| GlcCer |
|
ubiquitous |
|
GlcT-1/GCSUGCG |
|
precursor for GSLs biosynthesis, negative regulator for ceramide, axonal elongation of neuron,multidrug resistancy
|
|
|
|
|
|
|
|
| GalCer |
|
myelin, kidney, |
|
CGT |
|
insulative function of myelin |
|
|
|
|
|
|
|
| alpha GalCer |
|
unknown |
|
unknown |
|
ligand for NKT cell |
|
|
|
|
|
|
|
| FucCer |
|
colon and lung cancer |
|
unknown |
|
unknown |
|
|
|
|
|
|
|
| Cholesteryl glucoside |
|
human skin fibroblast |
|
unknown |
|
heat shock response |
|
|
|
|
|
|
|
| Cholesterylglucuronide |
|
human liver |
|
unknown |
|
unknown |
|
|
|
|
|
|
|
| Galactosyldiacyl glycerol |
|
sperm (seminolipid), intestine, etc. |
|
CGT |
|
sperm development |
|
|
|
|
|
|
|
| phosphatidylglucoside |
|
Radial glia, HL60 |
|
unknown |
|
raft component |
|
|
|
|
|
|
|
| NKT: natural Killer T |
|
|
|
|
|
|
|
近年の細胞生物学的な研究からスフィンゴ糖脂質は、細胞膜上のラフトと呼ばれる脂質ドメインに分布している(東氏によるグリコワード項を参照)。ラフト様の脂質ドメインは、トリトンX-100の不溶性、低比重の分画として生化学的に単離されている。得られる画分にはコレステロールやスフィンゴミエリンや糖脂質のスフィンゴ脂質が含まれる。重要なことは、膜糖脂質ドメインには、srcファミリーに属するリン酸化酵素が同時に回収されることである。この脂質ドメインは、細胞間接着や受容体を介したシグナル伝達に機能していると示唆されている。糖脂質のリッチなドメインは、病原体(コレラ菌、O157、HIV)やその毒素の結合に際しターゲットとして機能している。ラフトの実体に関しては依然として議論の対象であるが、ラフトの生化学的研究は新しい糖脂質、ホスファチジルグルコシド(PtdGlc)の発見をもたらした。この糖脂質は、発達期の脳組織では放射状グリア/星状体グリア細胞に特異的に発現している。興味深いことに、PtdGlcは、C18:0/C20:0の飽和脂肪酸のみで構成され、単一分子種として存在している(図1)。極めて異例の糖脂質であり、この糖脂質固有の機能に興味が持たれる(2)。
|
|
|
|
|
|
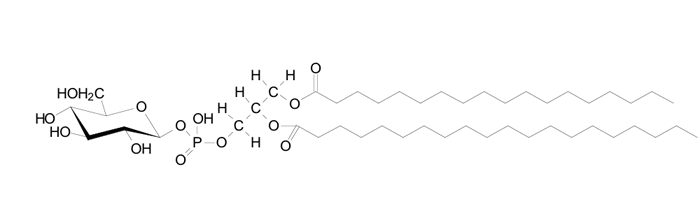
図 1 |
|
|
|
|
|
| 表 II Gene targeted mice: glycolipid functions at the whole animal level |
|
|
|
|
|
 |
|
|
|
|
|
| Gene disrupted |
|
Biochemical changes |
|
General
(conditional KO) |
|
|
|
|
|
 |
|
|
|
|
|
GlcCer synthase
(UGCG/GCS/GlcT-1) |
|
loss of all GSLs except GalCer |
|
embryonic leathality at E7.5,(UGCG/GCS/GlcT-1)(epidermis: loss of water barrierfunction, neural cells: neuronalcell degeneration)
|
|
|
|
|
|
| GalCer synthase (CGT) |
|
loss of GalCer and appearance of GlcCer in myelin, loss of seminolipid in sperm |
|
ataxia, loss of insulative function of myelin, sterility in male |
|
|
|
|
|
| Sulfatide synthase (CST) |
|
loss of sulfatide in myelin and of sulfated seminolipid in sperm |
|
similarity to CGT KO mouse |
|
|
|
|
|
| GM3 synthase |
|
appearance of GM1b and GD1alpha |
|
high sensitivity to insulin |
|
|
|
|
|
| GM2/GD2 (GalNAc-T) synthase |
|
loss of higher gangliosides (only GM3, GD3 and GT3) |
|
normal development, defect in nerve regeneration |
|
|
|
|
|
| GD3 synthase |
|
loss of higher gangliosides (only monosialo gangliosides) |
|
defect in nerve regeneration |
|
|
|
|
|
UDCG:UDP-Glc Ceramide Glucosyltransferase
CGT: Ceramide Galactosyltransferase
CST: Cerebroside Sulfotransferase |
|
|
|
|
|
|
|
|
スフィンゴ糖脂質の欠損したB16のメラノーマ細胞が確立された。この変異細胞はグルコシルセラミド合成活性が欠損している。この変異細胞を使った研究から、糖脂質合成は細胞の生存や増殖に、すくなくともこのメラノーマ細胞では関与していない事が示された。唯一のスフィンゴ脂質であるスフィンゴミエリンが糖脂質の肩代わりをしていると考えられる。同様に、スフィンゴ糖脂質は、ラフト様の膜ドメイン形成にも必須な構成要素ではない。これら研究結果から、試験管内でスフィンゴ糖脂質の機能を解明するのは困難である。現在では、糖脂質合成酵素のノックアウトマウスを使い、多細胞系、個体レベルでの機能解析に焦点が向けられている。現在までにいくつかのノックアウトマウスが得られている(表II)。驚いたことに、複雑なガングリオシド合成を破壊しても、マウスは無事に生まれ、重大な異常は認められない。GD3ガングリオシド、およびGM2/GD2ガングリオシド合成酵素の両者をノックアウトしたダブルノックアウトマウス(このマウスはGM3ガングリオシドのみを発現している)も無事生まれてくる。これらのノックアウトマウスを使った実験から、複雑なガングリオシドは細胞の分化には直接関与しておらず、むしろ神経組織でのホメオスタシス維持や再生に関与していることが明らかにされている(古川鋼一氏によるグリコワードの項を参照)。最近、てんかん症状を示すヒト患者のなかから、GM3生合成酵素欠損の症例が初めて発見された(3)。GM3ノックアウトマウスでは、インスリン高感受性を示す。
1999年には、UGCGノックアウトマウスが作られた。このミュータントマウスは、GalCerを除く全てのスフィンゴ糖脂質を欠いている故、スフィンゴ糖脂質の一般的機能を知る上で貴重な情報を与えてくれる。詳細は、平林の“グリコワード“グルコシルセラミド合成酵素の項を参照。ガラクトシルセラミド合成酵素のノックアウトマウスが、1996年に最初に作られている。UGCGとは対照的に、このノックアウトマウスは無事生まれ、ミエリン構造においても際だった異常性は認められない。しかしながら、全身の震えや運動失調が現れ、このクラスのスフィンゴ脂質がミエリン機能に重要な役割を果たしていることが示された。最近の詳細な研究により、ミエリンのパラノーダルとよばれる領域に異常のあることが示されている。同じノックアウトマウスにより、同一ガラクトース転移酵素で合成されるセミノリピドが精子の発達に必須であることが示されている。
以上記した様に、糖脂質研究はポストシークエンス時代のライフサイエンス、特に脳科学領域において極めて重要であり、今後の発展が期待される。
|
|
|
|
|
|
平林 義雄
(理化学研究所脳科学総合研究センター・平林研究ユニット) |
|
|
|
|
|
| References |
(1) |
Hirabayashi Y, Ichikawa S: Roles of glycolipids and sphingolipids in biological membrane: The Frontiers in Molecular Biology Series (Eds, Fukuda, M., Hindsgaul, O, IRL Press at Oxford Press) (1999) pp220-248 |
|
(2) |
Kobayashi T, Takahashi M, Nagatsuka Y, Hirabayashi Y, Biol Pharm Bull29, 1526-1531, 2006 |
|
(3) |
Simpson et al, Nat Genet36, 1225-1229, 2004 |
|
(4) |
Yamashita T et al, Proc Natl Acad Sci U S A, 100, 3445-3449, 2003 |
|
|
|
|
|
| 2007年 3月 19日 |
|
|
|
|
|
|






