

 |
 |
生体膜糖脂質の機能 |
 |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| (Update Issue: 2007年3月19日) | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
 |
糖脂質は普遍的に細胞膜に存在している。哺乳動物のガングリオシドを含めた主要糖脂質のほとんどは疎水性のセラミドのグルコース化を触媒するグルコシルセラミド合成酵素(GlcT-1, UGCG) から合成されてくるスフィンゴ糖脂質(GSL)である。セラミドのガラクトシル化により合成されるガラクトシルセラミドは、ミエリン膜の特徴的な脂質として存在する。グリセロ型の糖脂質は、組織特異的に存在する。例えば、精巣にはガラクトシルアルキルアシルグリセリド(セミノリピド)、ヒトの臍帯血からホスファチジルグルコースが見いだされている(表1)。コレステロールグルコシドは、ヒトの細胞や肝臓組織に見いだされている。 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 近年の細胞生物学的な研究からスフィンゴ糖脂質は、細胞膜上のラフトと呼ばれる脂質ドメインに分布している(東氏によるグリコワード項を参照)。ラフト様の脂質ドメインは、トリトンX-100の不溶性、低比重の分画として生化学的に単離されている。得られる画分にはコレステロールやスフィンゴミエリンと糖脂質のスフィンゴ脂質が含まれる。重要なことは、膜糖脂質ドメインには、srcファミリーに属するリン酸化酵素が同時に回収されることである。この脂質ドメインは、細胞間接着や受容体を介したシグナル伝達に機能していると示唆されている。糖脂質のリッチなドメインは、病原体(コレラ菌、O157、HIV)やその毒素の結合に際しターゲットとして機能している(図1)。 |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
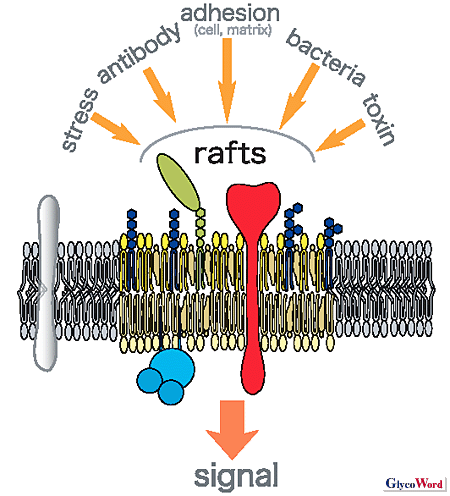 Fig.1 |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
スフィンゴ糖脂質の欠損したB16のメラノーマ細胞が確立された。この変異細胞はグルコシルセラミド合成活性が欠損している。この変異細胞を使った研究から、糖脂質合成は細胞の生存や増殖に、すくなくともこのメラノーマ細胞では全く関与していない事が示された。唯一のスフィンゴ脂質であるスフィンゴミエリンが糖脂質の肩代わりをしていると考えられる。同様に、スフィンゴ糖脂質は、ラフト様の膜ドメイン形成にも必須な構成要素ではない。これら試験管内の研究結果から、スフィンゴ糖脂質は細胞の基本的な機能に関わっていない様に思われる。従って、今後のスフィンゴ糖脂質研究は、多細胞系、個体レベルでの機能解析に焦点が向けられている。しかしながら、現在までスフィンゴ糖脂質合成酵素が関係する遺伝疾患は報告されておらず、ヒトにおける生理機能は不明である。 スフィンゴ糖脂質生理機能の謎を解決する目的で、遺伝子相同組み替え系により目的の遺伝子を破壊する方法が導入され、現在までにいくつかのノックアウトマウスが得られている(表II)。驚いたことに、複雑なガングリオシド合成を破壊しても、マウスは無事に生まれ、重大な異常は認められない。GD3ガングリオシド、およびGM2/GD2ガングリオシド合成酵素の両者をノックアウトしたダブルノックアウトマウス(このマウスはGM3ガングリオシドのみを発現している)も無事生まれてくる。これらのノックアウトマウスを使った実験から、複雑なガングリオシドは細胞の分化には直接関与しておらず、むしろ神経組織でのホメオスタシス維持や再生に関与していることが明らかにされている(古川鋼一氏によるグリコワードの項を参照)。ごく最近、Kawaiらにより、ダブルノックアウトマウスは音に極めて感受性が高く、音刺激で突然死を起こすことが報告されている。 1999年には、UGCGノックアウトマウスが作られた。このミュータントマウスは、GalCerを除く全てのスフィンゴ糖脂質を欠いている故、スフィンゴ糖脂質の一般的機能を知る上で貴重な情報を与えてくれる。ノックアウトマウスは胎児期(7.5日)に死んでしまう。この結果は、スフィンゴ糖脂質合成は、多細胞系の発達に必須であることを明確に示している。UGCGミュータントマウスは、外胚葉でのアポトーシスの昂進が見られる。しかし、何故UGCGの破壊により、アポトーシスが昂進するのかはっきりとは分かっていない。その理由として、UGCGには少なくとも2つの重要な機能があると考えられるからである。一つは、セラミドを糖化することにより細胞内のセラミド量をネガティブに調節している。もう一つは、UGCGの産物であるグルコシルセラミドが細胞増殖のポジティブな調節機構に関与しているからである。又、ラフトとの関係も不明である。 ガラクトシルセラミド合成酵素のノックアウトマウスが、1996年に最初に作られている。UGCGとは対照的に、このノックアウトマウスは無事生まれてきて、ミエリンの主要なスフィンゴ糖脂質であるガラクトシルセラミド、スルファチドの両者が完全に欠損しているにもかかわらず、ミエリン構造においても際だった異常性は認められない。しかしながら、全身の震えや運動失調が現れ、このクラスのスフィンゴ脂質脂質がミエリン機能に重要な役割を果たしていることが明らかとなった。同じノックアウトマウスによりガラクトース転移酵素で合成されるセミノリピドが精子の発達に必須であることが示されている。 以上記した様に、スフィンゴ糖脂質研究は、ポストシークエンス時代のライフサイエンスにおいて極めて重要で可能性を秘めた研究領域として認識されつつある。 |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 平林 義雄、大須賀 壮 (理化学研究所脳科学総合研究センター・神経回路メカニズム研究グループ) |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 2002年 6月 15日 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||