|
| References |
(1) |
Blix FG, Gottschalk A, Klenk E: Proposed nomenclature in the field of neuraminic and sialic acids. Nature, 179, 1088, 1957
|
|
(2) |
Nadano D, Iwasaki M, Endo S, Kitajima K, Inoue S, Inoue Y: A naturally occurring deaminated neuraminic acid, 3-deoxy-D-glycero-D-galacto-nonulosonic acid (KDN). Its unique occurrence at the nonreducing ends of oligosialyl chains in polysialoglycoprotein of rainbow trout eggs. J Biol. Chem., 261, 11550-11557, 1986
|
|
(3) |
Angata T, Varki A: Chemical diversity in the sialic acids and related alpha-keto acids:an evolutionary perspective. Chem. Rev., 102, 439-469, 2002 |
|
(4) |
Hara S, Takemori Y, Yamaguchi M, Nakamura M, Ohkura Y: Fluorometric high-performance liquid chromatography of N-acetyl- and N-glycolylneuraminic acids and its application to their microdetermination in human and animal sera, glycoproteins, and glycolipids. Anal Biochem., 164, 138-145, 1987 |
|
(5) |
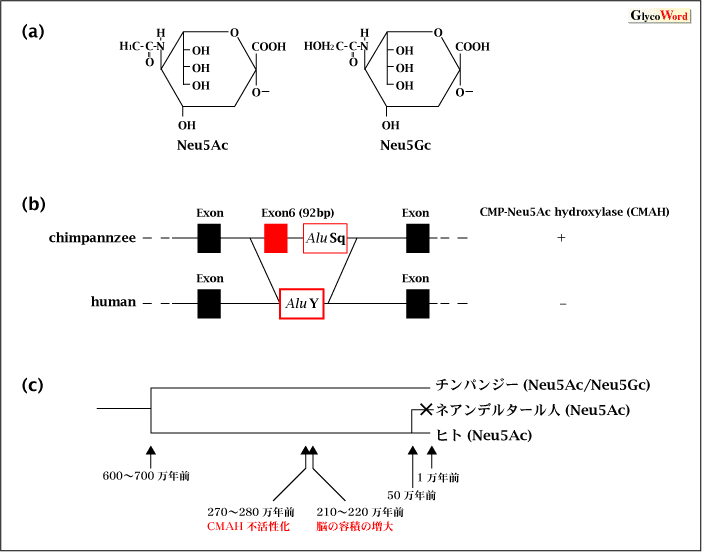
Chou HH, Hayakawa T, Diaz S, Krings M, Indriati E, Leakey M, Paabo S, Satta Y, Takahata N, Varki A: Inactivation of CMP-N-acetylneuraminic acid hydroxylase occurred prior to brain expansion during human evolution. Proc. Natl. Acad. Sci. USA, 99, 11736-11741, 2002 |
|
(6) |
Irie A, Koyama S, Kozutsumi Y, Kawasaki T, Suzuki A: The molecular basis for the absence of N-glycolylneuraminic acid in humans. J. Biol. Chem., 273, 15866-15871, 1998 |
|
(7) |
Chou HH, Takematsu H, Diaz S, Iber J, Nickerson E, Wright KL, Muchmore EA, Nelson DL, Warren ST, Varki A: A mutation in human CMP-sialic acid hydroxylase occurred after the Homo-Pan divergence. Proc. Natl. Acad. Sci. USA, 95. 11751-11756, 1998 |
|
(8) |
Hayakawa T, Satta Y, Gagneux P, Varki A, Takahata N: Alu-mediated inactivation of the human CMP-N-acetylneuraminic acid hydroxylase gene. Proc. Natl. Acad. Sci. USA, 98, 11399-11404, 2001 |
|
(9) |
Tangvoranuntakul P, Gagneux P, Diaz S, Bardor M, Varki N, Varki A, Muchmore E: Human uptake and incorporation of an immunogenic nonhuman dietary sialic acid. Proc. Natl. Acad. Sci. USA, 100, 12045-12050, 2003 |
|
(10) |
Schwarzkopf M, Knobeloch KP, Rohde E, Hinderlich S, Wiechens N, Lucka L, Horak I, Reutter W, Horstkorte R: Sialylation is essential for early development in mice. Proc. Natl. Acad. Sci. USA, 99, 5267-5270, 2002 |
|
(11) |
Varki A. in Essentials of glycobilogy (Varki A, Cumminings R, Esko J, Freeze H, Hart G. and Marth J. eds), pp195-209, 1999 |
|
|
|
|
|
|
|
|